全球范圍內(nèi)急性和慢性肝病負(fù)擔(dān)沉重,亟需安全有效的再生療法來(lái)補(bǔ)充或延緩肝移植。間充質(zhì)干細(xì)胞(MSCs)已被公認(rèn)為用途廣泛的生物制劑,主要通過(guò)旁分泌信號(hào)傳導(dǎo)調(diào)節(jié)炎癥、逆轉(zhuǎn)纖維化并促進(jìn)肝臟修復(fù)。
全球肝病的沉重負(fù)擔(dān)與主要類(lèi)型:肝臟疾病是全球重要的公共衛(wèi)生挑戰(zhàn),約占全球死亡總數(shù)的4%,每年導(dǎo)致約150萬(wàn)人死亡。慢性肝病是發(fā)病和死亡的主要原因,2021年全球肝硬化病例估計(jì)達(dá)5840萬(wàn)例。肝病相關(guān)死亡的主要誘因包括慢性乙型及丙型肝炎病毒感染所致的肝硬化、酒精相關(guān)性肝病、代謝功能障礙相關(guān)脂肪性肝病(MASLD)以及肝細(xì)胞癌,而急性肝損傷(ALI)所占比例相對(duì)較小。

肝臟再生潛力與傳統(tǒng)治療局限:肝臟雖具有顯著的再生能力,但慢性損傷會(huì)破壞這一過(guò)程,導(dǎo)致持續(xù)炎癥、纖維化和血管異常,最終形成阻礙再生的病理性微環(huán)境。對(duì)于終末期肝病,原位肝移植是當(dāng)前唯一的根治性手段,但其應(yīng)用受到供體嚴(yán)重短缺、高昂費(fèi)用、需終身免疫抑制治療及相關(guān)并發(fā)癥(如感染、代謝性疾病和移植物排斥)的嚴(yán)重限制,影響了患者的長(zhǎng)期生存與生活質(zhì)量。
干細(xì)胞再生療法的前景與挑戰(zhàn):基于上述局限,調(diào)節(jié)肝臟微環(huán)境的再生療法成為備受關(guān)注的策略,其中間充質(zhì)干細(xì)胞(MSCs)及其衍生物因具有多機(jī)制促再生潛力而展現(xiàn)出廣闊前景。雖然MSCs療法為急性肝損傷、肝硬化等疾病提供了生物學(xué)依據(jù),但其來(lái)源、培養(yǎng)與給藥策略的差異要求建立標(biāo)準(zhǔn)化方案和臨床效價(jià)檢測(cè)方法,以確保治療可靠性。
間充質(zhì)基質(zhì)/干細(xì)胞療法在肝臟再生中的應(yīng)用:現(xiàn)狀與未來(lái)方向
在此背景下,近期,國(guó)際醫(yī)學(xué)科學(xué)雜志刊發(fā)了一篇“間充質(zhì)基質(zhì)/干細(xì)胞療法在肝臟再生中的應(yīng)用:現(xiàn)狀與未來(lái)方向”的研究綜述[1]。

該研究對(duì)MSCs的生物學(xué)特性、肝臟再生以及基于細(xì)胞的療法與基于EVs的療法,包括給藥途徑、劑量、質(zhì)量和安全性進(jìn)行了逐一綜述。此外,該研究表明未來(lái)的研究方向?qū)?cè)重于生物標(biāo)志物、多中心臨床試驗(yàn)以及用于可擴(kuò)展的個(gè)性化肝臟再生的工程化MSC/EV平臺(tái)。
間充質(zhì)干細(xì)胞的生物學(xué)和來(lái)源依賴(lài)性特性
基本生物學(xué)特性與定義:根據(jù)國(guó)際細(xì)胞治療協(xié)會(huì)的定義,間充質(zhì)干細(xì)胞的基本生物學(xué)特性包括:在塑料表面貼壁生長(zhǎng);表達(dá)特定表面標(biāo)志物(CD73、CD90、CD105陽(yáng)性,而造血標(biāo)志物陰性);具備體外成骨、成脂和成軟骨的三系分化潛能。術(shù)語(yǔ)上,“間充質(zhì)基質(zhì)細(xì)胞”更貼近這一定義,而“間充質(zhì)干細(xì)胞”通常需體內(nèi)自我更新和多能性的證據(jù),但研究中兩者常混用。
主要組織來(lái)源及其特性:MSCs最初從骨髓中分離,現(xiàn)已廣泛發(fā)現(xiàn)于脂肪、臍帶、胎盤(pán)等成人與圍產(chǎn)期組織中。其特性受來(lái)源、供體年齡和培養(yǎng)條件影響,導(dǎo)致顯著的異質(zhì)性,這也是治療標(biāo)準(zhǔn)化面臨的主要挑戰(zhàn)。
- 骨髓來(lái)源MSCs(BM-MSCs):具有較強(qiáng)的成骨和免疫調(diào)節(jié)能力,但獲取過(guò)程有創(chuàng),且細(xì)胞數(shù)量有限。
- 脂肪來(lái)源MSCs(AD-MSCs):易于從吸脂物中大量獲取,分泌組富含生長(zhǎng)因子和EVs,能有效促進(jìn)血管生成、細(xì)胞增殖與遷移,適合規(guī)模化生產(chǎn)。
- 圍產(chǎn)期來(lái)源MSCs(如臍帶、胎盤(pán)):具有低免疫原性、高增殖潛能以及顯著的抗纖維化和抗炎特性,例如通過(guò)分泌基質(zhì)金屬蛋白酶(MMPs)抑制纖維化并調(diào)節(jié)免疫反應(yīng),在再生醫(yī)學(xué)中展現(xiàn)出獨(dú)特優(yōu)勢(shì)。
iPSC衍生MSCs及挑戰(zhàn):除天然組織來(lái)源外,MSCs也可由誘導(dǎo)多能干細(xì)胞(iPSC)定向分化獲得。iPSC衍生的MSCs表面標(biāo)志物與天然MSCs相似,且能長(zhǎng)期擴(kuò)增,但可能存在基因組異常和潛在的致瘤風(fēng)險(xiǎn),需要嚴(yán)格的質(zhì)量控制。
總體而言,MSCs的來(lái)源依賴(lài)性體現(xiàn)在其增殖能力、分泌組組成、免疫調(diào)節(jié)活性和分化傾向上,這些差異決定了其在肝臟疾病等具體應(yīng)用中的適用性。表1總結(jié)了與肝臟應(yīng)用相關(guān)的間充質(zhì)干細(xì)胞的來(lái)源依賴(lài)性特性。
| 特征 | 骨髓間充質(zhì)干細(xì)胞 | AD-MSCs | 圍產(chǎn)期間充質(zhì)干細(xì)胞 | iMSCs |
|---|---|---|---|---|
| 組織 來(lái)源 | 骨髓 | 脂肪組織 | 華通氏膠、臍帶血、胎盤(pán) | iPSC衍生 |
| 擴(kuò)散能力 | 低( 占有核細(xì)胞的 0.001%–0.01%) | 高的 | 非常高 | 無(wú)限 |
| 提取方法 | 侵入性抽吸 技術(shù) | 微創(chuàng)吸脂 術(shù) | 無(wú)創(chuàng)采集圍產(chǎn)期組織 | 復(fù)雜的制造 過(guò)程 |
| 免疫學(xué)特性 | 強(qiáng) 免疫調(diào)節(jié) 作用 | 免疫調(diào)節(jié)劑 | 免疫原性低,具有顯著的抗炎和抗纖維化作用 | 與天然間充質(zhì)干細(xì)胞類(lèi)似 |
| 功能特性 | 具有強(qiáng)大的 成骨潛能、免疫調(diào)節(jié)作用,并已開(kāi)展廣泛的臨床 研究 | 高效增殖、 強(qiáng)效促再生 分泌組、高細(xì)胞產(chǎn)量,適合規(guī)模化生產(chǎn) | 保留原始表型;干細(xì)胞特性標(biāo)記物(如 OCT4 和 SOX2)表達(dá)升高; 可直接用于異體移植。 | 表面標(biāo)志物和 功能特征與天然間充質(zhì)干細(xì)胞相似; 基因組不穩(wěn)定、 具有致瘤風(fēng)險(xiǎn)、 生產(chǎn)工藝復(fù)雜 |
間充質(zhì)干細(xì)胞助力肝臟再生中的作用機(jī)制是什么?
間充質(zhì)干細(xì)胞(MSCs)通過(guò)多方面的旁分泌、免疫調(diào)節(jié)、抗纖維化、代謝和血管生成機(jī)制支持肝臟修復(fù)。MSCs協(xié)調(diào)肝臟微環(huán)境中的多種再生通路,并通過(guò)這些機(jī)制促進(jìn)組織修復(fù)(圖1,表2)。
- 營(yíng)養(yǎng)支持與直接促增殖:分泌肝細(xì)胞生長(zhǎng)因子(HGF)、胰島素樣生長(zhǎng)因子-1(IGF-1)等,直接促進(jìn)肝細(xì)胞增殖與存活。
- 免疫調(diào)節(jié):釋放細(xì)胞因子,抑制促炎性T細(xì)胞和M1型巨噬細(xì)胞,同時(shí)激活調(diào)節(jié)性T細(xì)胞(Tregs)和抗炎的M2型巨噬細(xì)胞,從而減輕局部炎癥。
- 抗纖維化:通過(guò)下調(diào)轉(zhuǎn)化生長(zhǎng)因子-β1(TGF-β1)等因子,抑制肝星狀細(xì)胞活化,減少細(xì)胞外基質(zhì)過(guò)度沉積。
- 促進(jìn)血管生成:分泌血管內(nèi)皮生長(zhǎng)因子(VEGF)等,改善損傷區(qū)域的血液循環(huán)。
- 細(xì)胞外囊泡(EVs)介導(dǎo)的調(diào)控:MSCs釋放的EVs可遞送功能性RNA、蛋白質(zhì),甚至進(jìn)行線粒體轉(zhuǎn)移,直接恢復(fù)受損肝細(xì)胞的代謝功能。

| 機(jī)制 | 關(guān)鍵因素 | 主要功能 | 參考 |
|---|---|---|---|
| 旁分泌/營(yíng)養(yǎng) | HGF、VEGF、IGF-1、IL-6 | 促進(jìn)肝細(xì)胞增殖,抑制細(xì)胞凋亡,增強(qiáng)組織灌注 | [ 56 , 57 , 58 ] |
| 免疫學(xué) | CD8 + T細(xì)胞、NK細(xì)胞和B細(xì)胞數(shù)量減少;M2巨噬細(xì)胞極化;前列腺素誘導(dǎo)調(diào)節(jié)性樹(shù)突狀細(xì)胞 | 抑制免疫反應(yīng),促進(jìn)抗炎環(huán)境,增強(qiáng)組織修復(fù) | [ 47 , 48 , 49 , 59 ] |
| 抗纖維化 | miR-378c(外泌體),TGF-β1抑制 | 抑制肝星狀細(xì)胞活化和纖維化 | [ 50 , 51 ] |
| 代謝 | 通過(guò)隧道納米管進(jìn)行線粒體轉(zhuǎn)移 | 恢復(fù)肝臟氧化能力和脂質(zhì)代謝 | [ 54 ] |
| 血管生成 | 血管緊張素-1、血管緊張素-2、血管內(nèi)皮生長(zhǎng)因子 | 增強(qiáng)肝臟再生過(guò)程中的血管生成和氧氣輸送 | [ 53 ] |
| 細(xì)胞外囊泡介導(dǎo)/旁分泌 | MicroRNA(miR-19b、miR-122、miR-124、miR-182-5p、miR-148a)、蛋白質(zhì)(DDX5、CAMKK1) | 調(diào)節(jié)受體細(xì)胞行為,無(wú)需細(xì)胞移植即可恢復(fù)肝功能 | [ 51 , 52 , 55 , 60 , 61 , 62 , 63 ] |
這些機(jī)制相互重疊、協(xié)同作用,形成一個(gè)動(dòng)態(tài)網(wǎng)絡(luò)。其主導(dǎo)地位隨肝損傷與修復(fù)階段而變化:損傷早期以快速免疫調(diào)節(jié)為主,為修復(fù)創(chuàng)造穩(wěn)定環(huán)境;組織重塑階段抗纖維化作用凸顯;長(zhǎng)期來(lái)看,代謝支持和促血管生成效應(yīng)則持續(xù)促進(jìn)功能與結(jié)構(gòu)的恢復(fù)。
基于細(xì)胞與無(wú)細(xì)胞的治療肝臟疾病的策略是什么?
基于細(xì)胞與無(wú)細(xì)胞的治療肝臟疾病策略,核心區(qū)別在于是否使用活的間充質(zhì)干細(xì)胞(MSC)本身。基于細(xì)胞的策略指直接輸注活體MSCs。這些細(xì)胞被視為“智能藥物工廠”,能夠在體內(nèi)存活、歸巢至損傷部位,并根據(jù)局部微環(huán)境動(dòng)態(tài)調(diào)整其旁分泌(如生長(zhǎng)因子、細(xì)胞外囊泡)和免疫調(diào)節(jié)功能,實(shí)現(xiàn)個(gè)體化的、自適應(yīng)的治療響應(yīng)。然而,該策略面臨活細(xì)胞固有的挑戰(zhàn),包括靜脈輸注后的肺部滯留、隨培養(yǎng)擴(kuò)增而下降的歸巢能力和潛在的遺傳不穩(wěn)定性風(fēng)險(xiǎn)。
無(wú)細(xì)胞的策略則主要利用MSCs分泌的細(xì)胞外囊泡(EVs)。EVs是富含蛋白質(zhì)、RNA等生物活性物質(zhì)的納米級(jí)囊泡,可視為MSC治療效應(yīng)的“標(biāo)準(zhǔn)化包裹”。它們能再現(xiàn)MSCs的抗炎、抗纖維化和促再生作用,同時(shí)規(guī)避了活細(xì)胞移植的腫瘤風(fēng)險(xiǎn)和免疫排斥問(wèn)題,且更易于儲(chǔ)存、滅菌和劑量標(biāo)準(zhǔn)化。但EVs的功能是固定的,無(wú)法像活細(xì)胞那樣動(dòng)態(tài)適應(yīng)體內(nèi)變化,其大規(guī)模生產(chǎn)與質(zhì)控也面臨技術(shù)挑戰(zhàn)。
因此,當(dāng)前形成了一種互補(bǔ)范式:在需要復(fù)雜、動(dòng)態(tài)免疫調(diào)節(jié)(如嚴(yán)重炎癥或自身免疫相關(guān)肝病)時(shí),優(yōu)先使用活的MSCs;而當(dāng)治療目標(biāo)明確為標(biāo)準(zhǔn)的抗炎和抗纖維化時(shí),則可選用更安全、易控的EVs制劑。治療時(shí)還需綜合考慮細(xì)胞/囊泡來(lái)源、遞送途徑和疾病階段等因素以?xún)?yōu)化療效。
間充質(zhì)干細(xì)胞治療肝病的給藥途徑和劑量對(duì)治療效果的影響
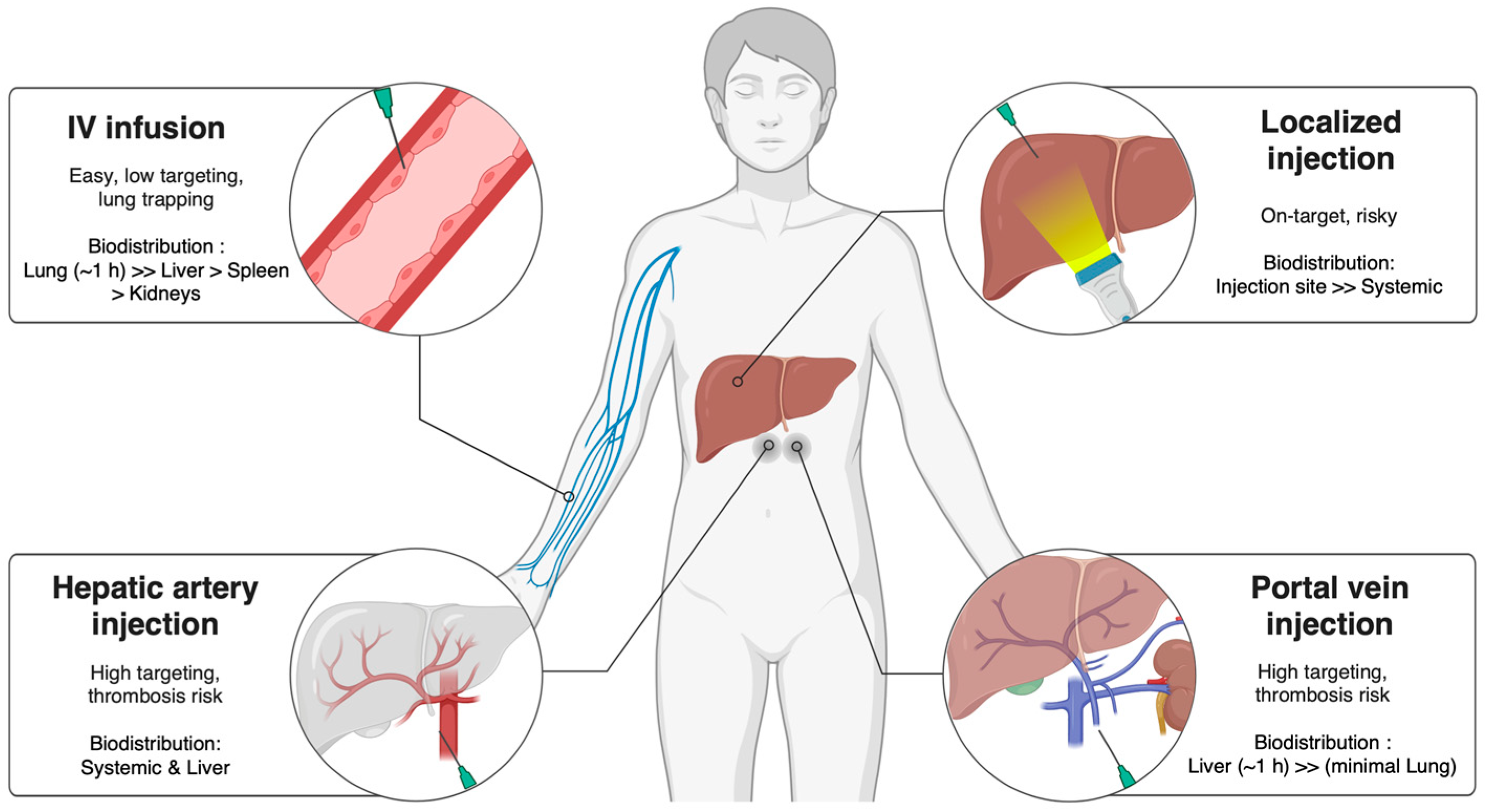
給藥途徑是影響間充質(zhì)干細(xì)胞治療肝臟疾病效果和安全性的關(guān)鍵因素。常見(jiàn)的途徑包括外周靜脈輸注、門(mén)靜脈/肝動(dòng)脈注射以及局部肝內(nèi)注射。
靜脈注射是最簡(jiǎn)單、創(chuàng)傷最小的方法,因此方便且通常是首選。但大量細(xì)胞會(huì)滯留于肺部,導(dǎo)致肝臟靶向性降低。
相比之下,經(jīng)門(mén)靜脈或肝動(dòng)脈的直接肝臟給藥能顯著提高細(xì)胞在肝內(nèi)的局部濃度和滯留率,但屬于侵入性操作,對(duì)伴有門(mén)脈高壓和凝血功能障礙的肝硬化患者存在較高出血和血栓風(fēng)險(xiǎn)。局部影像引導(dǎo)下的注射能精準(zhǔn)作用于特定病灶,但不適用于彌漫性肝損傷,MSC和EV在治療肝病中的遞送途徑總結(jié)于圖2中。
治療劑量和方案需根據(jù)疾病類(lèi)型和階段進(jìn)行個(gè)體化調(diào)整。在急性肝損傷的臨床前模型中,常用有效劑量為1–5×10?個(gè)細(xì)胞/公斤體重,其中中等劑量效果最佳,更高劑量未必增效。對(duì)于慢性肝損傷或肝纖維化,典型劑量范圍為0.5–3×10?個(gè)細(xì)胞/公斤體重,且研究顯示重復(fù)給藥通常比單次給藥效果更優(yōu),表明存在累積治療效應(yīng)。
若使用MSC來(lái)源的細(xì)胞外囊泡,常用劑量范圍為10?–1012個(gè)顆粒/公斤或50–600微克蛋白質(zhì),中等劑量往往能產(chǎn)生最佳治療反應(yīng),表3詳細(xì)總結(jié)了適應(yīng)癥特異性劑量范圍和劑量-反應(yīng)趨勢(shì)。這些發(fā)現(xiàn)強(qiáng)調(diào)了仔細(xì)滴定和藥效學(xué)監(jiān)測(cè)的必要性,以?xún)?yōu)化治療效果。
| 肝損傷模型 | 治療 | 劑量范圍 | 行政路線 | 劑量反應(yīng) | 參考 |
|---|---|---|---|---|---|
| ALI(小鼠/大鼠) | 間充質(zhì)干細(xì)胞 | 1–5 × 10?個(gè)細(xì)胞/千克 | 第四 | 1–2 × 10? :效果差; 2–4 × 10? :效果最佳/中等;>4 × 10? :效果停滯或略有下降 | [ 97 , 101 ] |
| CLI/纖維化(小鼠/大鼠) | 間充質(zhì)干細(xì)胞 | 0.5–3 × 10? 個(gè)細(xì)胞/千克(或 1–20 × 10?個(gè)總細(xì)胞) | IV,IP | 0.5–1 × 10? :效果不佳; 1–3 × 10? :效果中等; >3 × 10? :無(wú)進(jìn)一步改善 | [ 101 , 105 ] |
| 失代償期 肝硬化(人類(lèi),早期臨床) | 間充質(zhì)干細(xì)胞 | 5 × 10? – 2 × 10?個(gè)細(xì)胞/輸注 | 第四 | 5–10 × 10? :效果不佳; 1–2 × 10? :中等/最佳; 更高劑量:未觀察到額外益處 | [ 104 ] |
| 肝損傷(小鼠/大鼠) | MSC-EVs | 10? – 1012個(gè)顆粒/千克或 50–600 微克蛋白質(zhì) | 第四 | 10? – 3 × 101? 個(gè)顆粒(或 50–150 μg):低效應(yīng); 3 × 101? –1 × 1011個(gè)顆粒(150–300 μg):中等效應(yīng); >1 × 1011 個(gè)顆粒(300–600 μg):平臺(tái)期 | [ 102 , 106 ] |
| 缺血性肝病/ 中風(fēng)模型 | MSC-EVs | 30–250 μg 蛋白質(zhì) | 第四 | 30–100 微克:效果較差;100–250 微克:效果中等/最佳;重復(fù)給藥可能進(jìn)一步增強(qiáng)效果 | [ 103 , 106 ] |
綜上所述,給藥途徑和劑量的選擇需要綜合權(quán)衡。途徑選擇需考慮靶向性、操作風(fēng)險(xiǎn)及疾病分布特點(diǎn)(局灶性或彌漫性),而劑量確定則需依據(jù)損傷的急慢性性質(zhì),并通過(guò)仔細(xì)的劑量滴定和藥效學(xué)監(jiān)測(cè)來(lái)優(yōu)化。理想的治療策略應(yīng)是在確保安全的前提下,通過(guò)最合適的途徑和劑量,使治療成分最大化地作用于肝臟靶點(diǎn)。
間充質(zhì)干細(xì)胞治療肝臟疾病基于生物材料增強(qiáng)治療效果的方式
生物材料作為先進(jìn)的遞送載體,能顯著改善間充質(zhì)干細(xì)胞(MSCs)及其細(xì)胞外囊泡(EVs)在肝臟疾病治療中的局限。通過(guò)水凝膠或可注射支架包裹MSCs/EVs進(jìn)行局部給藥,可以將治療成分有效錨定在肝臟靶點(diǎn),避免靜脈輸注后的肺部首過(guò)滯留和全身性清除,從而大幅提高局部濃度和滯留時(shí)間。
這些材料模擬細(xì)胞外基質(zhì),為MSCs提供了一個(gè)支持存活、增強(qiáng)旁分泌功能的三維微環(huán)境,并能緩釋EVs等活性物質(zhì),延長(zhǎng)治療窗口。這從根本上優(yōu)化了傳統(tǒng)給藥途徑的靶向性和效率,圖3總結(jié)了生物材料輔助策略在增強(qiáng)間充質(zhì)干細(xì)胞和細(xì)胞外囊泡治療肝病中的療效方面的應(yīng)用。

生物材料的應(yīng)用更進(jìn)一步,通過(guò)功能化設(shè)計(jì)實(shí)現(xiàn)了治療效果的精準(zhǔn)增強(qiáng)。
- 一方面,利用溫敏水凝膠等實(shí)現(xiàn)微創(chuàng)注射和原位成型,便于臨床操作。
- 另一方面,通過(guò)對(duì)載體進(jìn)行表面修飾(如連接靶向肝細(xì)胞的半乳糖配體)或?qū)SCs/EVs本身進(jìn)行工程化改造(如聚乙二醇化),可主動(dòng)引導(dǎo)它們向肝臟或特定細(xì)胞(如肝細(xì)胞)歸巢,減少脫靶效應(yīng)。
這些策略綜合提升了抗炎、抗纖維化和再生信號(hào)的傳遞效率,臨床前研究已證實(shí)其能協(xié)同增強(qiáng)MSC的治療效果,為實(shí)現(xiàn)更安全、強(qiáng)效和持久的肝臟修復(fù)提供了關(guān)鍵技術(shù)支撐。
間充質(zhì)干細(xì)胞治療肝臟疾病的臨床概況:安全性和有效性
使用間充質(zhì)干細(xì)胞治療肝臟疾病的早期臨床試驗(yàn)
多項(xiàng)早期臨床試驗(yàn)研究了自體或異體間充質(zhì)干細(xì)胞(MSC)療法在肝硬化、急性加重型慢性肝衰竭(ACLF)及其他肝功能失代償患者中的安全性和初步療效。在這些研究中,MSC輸注顯示出良好的安全性,未報(bào)告重大輸注相關(guān)不良事件或致瘤并發(fā)癥。
初步療效指標(biāo)包括肝功能參數(shù)的改善,例如血清白蛋白和膽紅素、凝血酶原時(shí)間以及終末期肝病模型(MELD)評(píng)分和Child-Pugh評(píng)分。
表4總結(jié)了MSC治療肝病的早期臨床研究,包括疾病適應(yīng)癥、MSC來(lái)源、給藥途徑、樣本量、隨訪時(shí)間、主要結(jié)局指標(biāo)和不良事件。
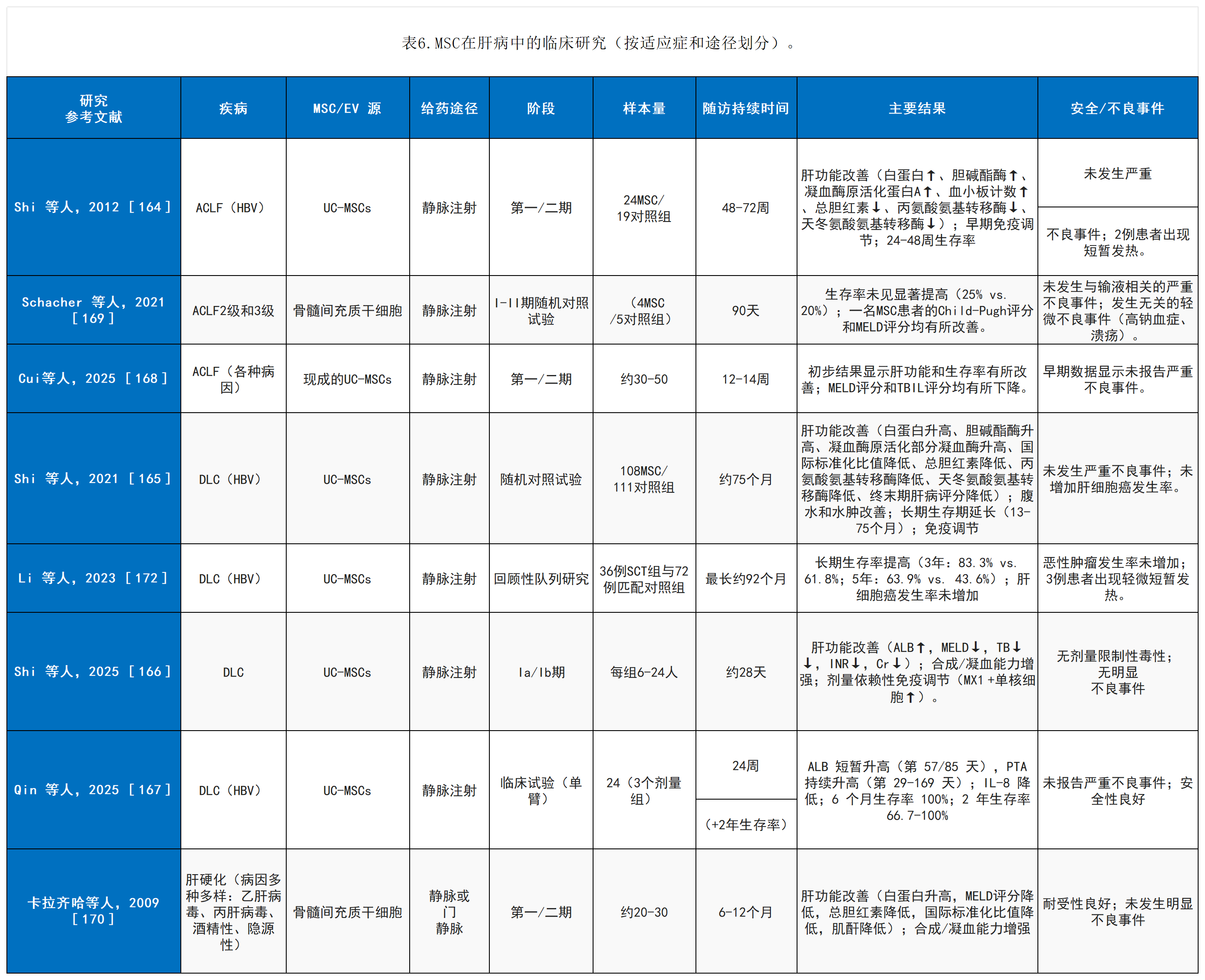
在這些早期短期試驗(yàn)中,臨床獲益通常僅在特定患者亞組中觀察到,例如病情較輕(MELD或Child-Pugh評(píng)分較低)、肝合成功能良好(基線白蛋白或凝血酶原活性較高)、乙型肝炎病毒相關(guān)病因或基線全身炎癥水平較低的患者。由于這些研究通常缺乏長(zhǎng)期隨訪,因此療效在6-12個(gè)月后的持久性仍不確定。這些短期研究中療效持續(xù)時(shí)間明顯有限或不一致,可能反映了肝損傷進(jìn)展、持續(xù)的炎癥環(huán)境和/或輸注的間充質(zhì)干細(xì)胞在不利的肝臟環(huán)境中植入或存活率有限。
重要的是,多項(xiàng)長(zhǎng)期隨訪研究報(bào)告了持續(xù)獲益,包括數(shù)年內(nèi)生存率和肝功能的改善。較高劑量的間充質(zhì)干細(xì)胞(MSC)(2×10?個(gè)細(xì)胞)和重復(fù)給藥(每周一次,持續(xù)3周)可改善肝功能,這體現(xiàn)在Child-Pugh評(píng)分和MELD評(píng)分的降低,以及MX1?單核細(xì)胞比例的降低。這些觀察結(jié)果表明,劑量、重復(fù)給藥和患者特征可能影響療效。需要更大規(guī)模的對(duì)照試驗(yàn)來(lái)證實(shí)這些臨床發(fā)現(xiàn)。
在各種間充質(zhì)干細(xì)胞(MSC)來(lái)源中,臍帶間充質(zhì)干細(xì)胞(UC-MSC)顯示出最穩(wěn)定的療效。短期至長(zhǎng)期隨訪結(jié)果顯示,血清白蛋白升高5-15g/L,凝血酶原活性提高10-20%,總膽紅素降低20-35%。MELD評(píng)分降低2-5分,Child-Pugh評(píng)分提高1-3分,長(zhǎng)期生存獲益可達(dá)75-92個(gè)月。
最常見(jiàn)的不良反應(yīng)是輕度短暫發(fā)熱,并觀察到劑量依賴(lài)性的免疫調(diào)節(jié)作用,包括MX1+單核細(xì)胞和IL-8的減少。BM-MSCs也改善了肝功能,白蛋白升高約5–10g/L,MELD評(píng)分降低約1–3分,總膽紅素降低約15–25%。然而,生存獲益并不穩(wěn)定,尤其是在隨訪時(shí)間較短的小型隨機(jī)對(duì)照試驗(yàn)中。靜脈和門(mén)靜脈給藥均耐受性良好,未報(bào)告嚴(yán)重不良事件。
總體而言,UC-MSCs似乎比BM-MSCs提供更持久的功能和生存獲益,而AD-MSCs的臨床數(shù)據(jù)非常有限,iMSCs僅進(jìn)行了臨床前研究。
間充質(zhì)干細(xì)胞治療肝臟疾病安全性怎么樣?以及緩解風(fēng)險(xiǎn)的方法有哪些?
間充質(zhì)干細(xì)胞(MSCs)治療肝臟疾病雖顯示出良好的總體安全性,但仍存在若干需謹(jǐn)慎管理的特定風(fēng)險(xiǎn)。
- 輸注相關(guān)反應(yīng):如短暫發(fā)熱、寒戰(zhàn)。
- 血栓栓塞風(fēng)險(xiǎn):尤其對(duì)肝硬化患者,可能與高細(xì)胞劑量或MSCs表達(dá)組織因子有關(guān)。
- 遺傳不穩(wěn)定與致瘤潛能:與長(zhǎng)期體外擴(kuò)增相關(guān)。
- 免疫致敏風(fēng)險(xiǎn):異體MSCs重復(fù)給藥可能誘發(fā)免疫反應(yīng)。
風(fēng)險(xiǎn)緩解策略包括:控制細(xì)胞劑量與輸注速度、采用抗凝方案、對(duì)細(xì)胞產(chǎn)品進(jìn)行嚴(yán)格的基因組穩(wěn)定性評(píng)估、排除活動(dòng)性惡性腫瘤患者。此外,采用無(wú)細(xì)胞的EVs策略可提供更高的理論安全邊際。優(yōu)化遞送方式(如局部注射)和加強(qiáng)患者篩選與治療后監(jiān)測(cè),也是平衡獲益與風(fēng)險(xiǎn)的關(guān)鍵。
表5總結(jié)了基于MSCs的療法在肝硬化和急性加重型慢性肝衰竭中報(bào)告的不良事件,包括常見(jiàn)和嚴(yán)重不良事件的發(fā)生率和嚴(yán)重程度。
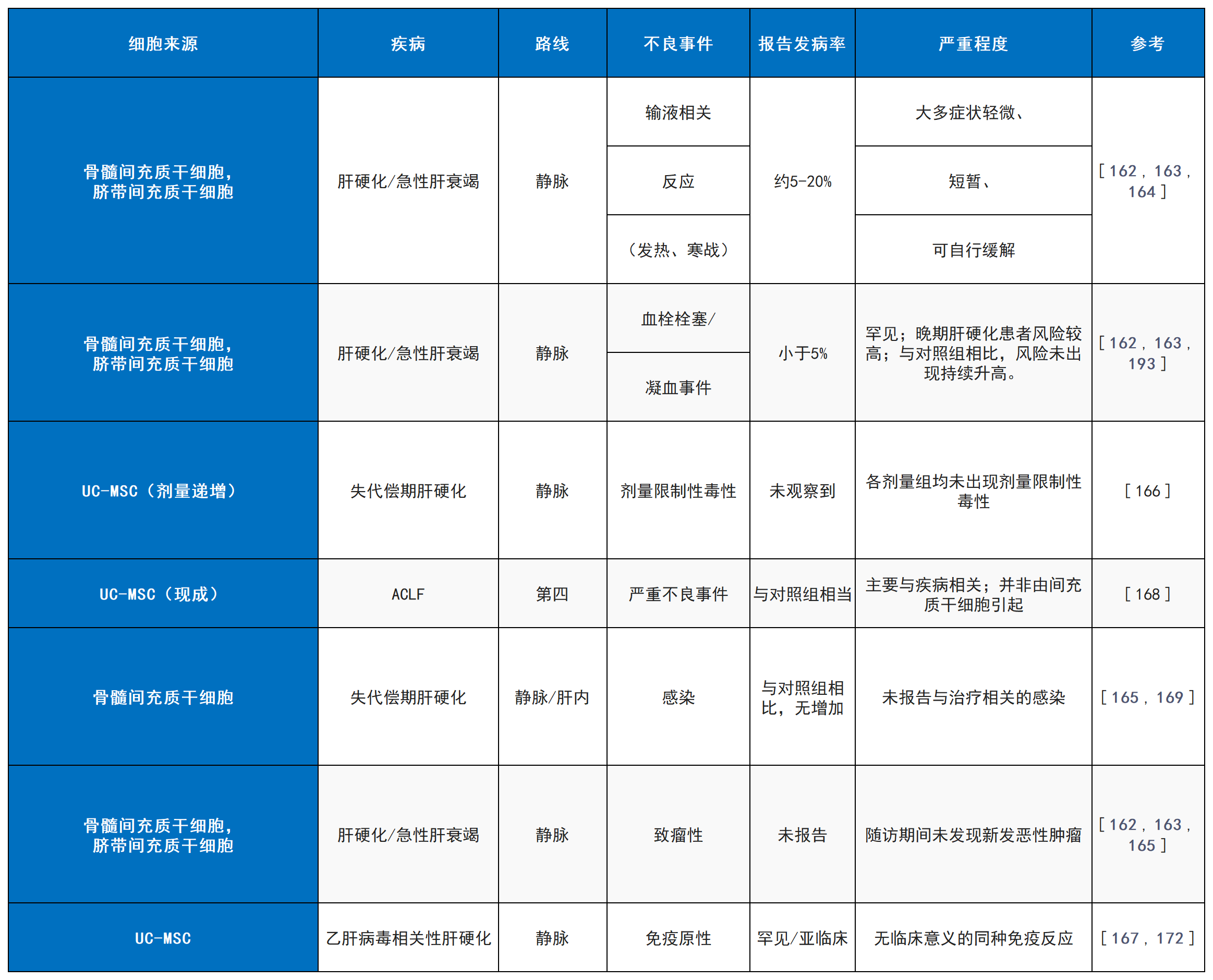
結(jié)論與未來(lái)方向
間充質(zhì)干細(xì)胞及其細(xì)胞外囊泡在再生肝病學(xué)領(lǐng)域展現(xiàn)出巨大潛力,有望恢復(fù)肝功能并減少對(duì)肝移植的需求。盡管臨床前與早期臨床研究結(jié)果鼓舞人心,但在治療方案標(biāo)準(zhǔn)化、效力驗(yàn)證和監(jiān)管路徑方面仍面臨挑戰(zhàn)。生物材料、EVs工程和精準(zhǔn)醫(yī)學(xué)的進(jìn)步,為開(kāi)發(fā)可擴(kuò)展、安全有效的療法提供了新途徑。
未來(lái)研究應(yīng)聚焦于:優(yōu)化符合藥品生產(chǎn)質(zhì)量管理規(guī)范(GMP)的生產(chǎn)工藝;建立并驗(yàn)證可靠的效力檢測(cè)方法;開(kāi)展設(shè)計(jì)嚴(yán)謹(jǐn)?shù)亩嘀行呐R床試驗(yàn);以及整合個(gè)體化醫(yī)療策略。建議的發(fā)展時(shí)間表包括:短期(1-2年)內(nèi)完善GMP生產(chǎn)與臨床前驗(yàn)證;中期(3-5年)推進(jìn)關(guān)鍵性多中心臨床試驗(yàn);長(zhǎng)期(5-10年)實(shí)現(xiàn)更廣泛的臨床轉(zhuǎn)化與應(yīng)用。
參考資料:
[1]:Choi, S.; Jeong, J. Mesenchymal Stromal/Stem Cell-Based Therapies for Liver Regeneration: Current Status and Future Directions. Int. J. Mol. Sci. 2026, 27, 619. https://doi.org/10.3390/ijms27020619
免責(zé)說(shuō)明:本文僅用于傳播科普知識(shí),分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專(zhuān)業(yè)建議。如有版權(quán)等疑問(wèn),請(qǐng)隨時(shí)聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信