近年來,干細胞療法,尤其是間充質干細胞(MSCs)干預策略,在腎移植受者中展現出獨特的免疫調節潛能,為實現移植腎長期存活乃至免疫耐受提供了新的技術路徑。與傳統免疫抑制方案相比,干細胞療法有望減輕藥物相關毒性、降低感染與腫瘤發生風險,進而改善受者生活質量與衛生經濟學效益。當前,該領域正從基礎探索加速向臨床轉化邁進。
基于47項臨床試驗的實證:干細胞療法或將終結腎移植后的長期“藥罐子”生活
近期,《Asian Journal of Surgery》發表了一篇題為《腎移植中干細胞療法的臨床試驗概況及文獻計量分析》的綜述。該研究整合了臨床試驗注冊數據與文獻計量學方法,系統描繪了該領域的研究現狀、演進脈絡與前沿趨勢,以期為后續研究與臨床決策提供參考[1]。

研究團隊對Trialtrove數據庫進行系統檢索,納入2000年1月至2025年8月間注冊的干細胞在腎移植中應用的臨床試驗,共篩選出47項合格研究。分析指標涵蓋試驗的時間趨勢、階段與狀態、地域分布、申辦方與資助類型及作用機制。由兩名研究人員獨立完成數據提取與交叉核對,對非結構化信息進行標準化處理,確保數據質量。
同時,基于Web of Science核心合集數據庫開展文獻計量分析,檢索時段為2005年1月至2025年7月,經兩輪人工篩選共納入1457篇相關文獻。
趨勢解析:發文量趨穩,試驗漸入后期
時間序列分析顯示,自2005年以來,相關出版物的數量呈快速上升趨勢,并在2015年達到峰值102篇(圖1A(a))。隨后,年產量穩定在70至100篇之間,表明該領域的研究活動持續活躍。
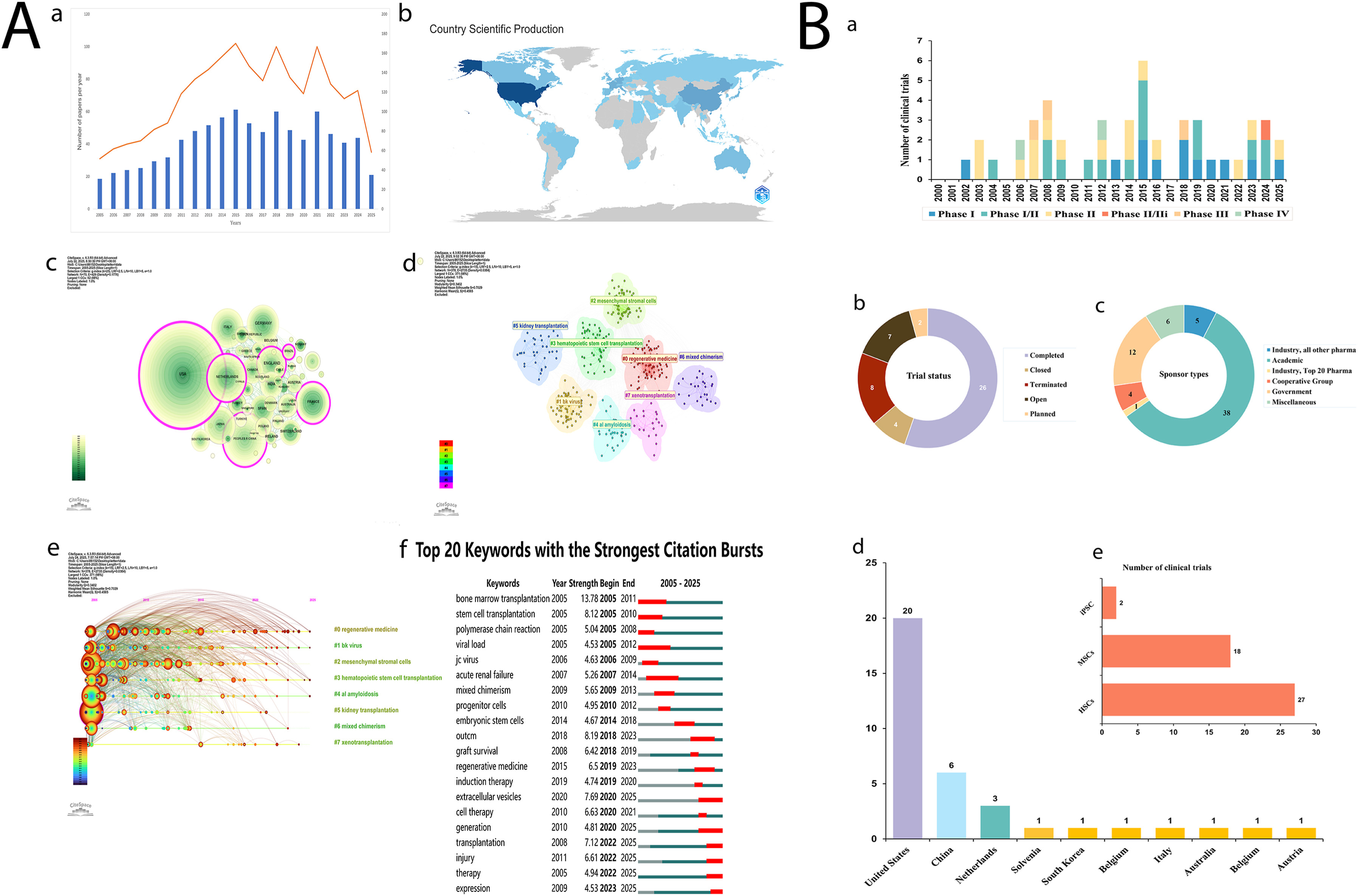
a.過去25年全球年度出版量及趨勢;b.按國家/地區劃分的出版物地理分布;c.出版國家/地區的分布圖;d.關鍵詞主題聚類分析;e.關鍵詞熱點的時間演變;f.新興關鍵詞(前20個)。(B)腎移植干細胞療法臨床試驗概覽。a.按啟動年份劃分的臨床試驗時間趨勢;b.臨床試驗的試驗狀態分布;c.臨床試驗資金來源分布;d.按國家/地區劃分的臨床試驗分布;e.干細胞療法類別分布;
與此同時,II期至IV期臨床試驗的數量顯著增加(圖1B(a)),表明研究重點已從基礎探索轉向臨床驗證和應用。在納入的47項試驗中,超過一半(26項,55.3%)已完成(圖1B(b))。研究經費主要來自學術機構(36項試驗),政府資助12項試驗(圖1B(c))。
地域版圖:美中領跑,科研基礎驅動轉化
地理分析顯示,美國是主要的研究中心(圖1A(b和c))。如圖1B(d)所示,美國以20項臨床試驗位居榜首,其次是中國和新西蘭。這表明,擁有雄厚科學基礎和完善監管體系的國家更有可能推進干細胞療法在腎移植領域的應用。就作用機制而言,造血干細胞(HSCs)應用最為廣泛,已有27項臨床試驗涉及其在誘導免疫耐受和減少對免疫抑制藥物依賴方面的應用(圖1B(e))。
熱點遷移:從基礎免疫學到細胞治療
關鍵詞共現網絡和時間趨勢分析表明,2005年至2014年(圖1A(e和f)),研究主要集中在“骨髓移植”、“混合嵌合體”和“祖細胞”等基礎免疫學問題上。2015年以后,研究熱點逐漸轉向轉化醫學領域,包括“再生醫學”、“胚胎干細胞”、“移植存活”和“誘導治療”。
這表明干細胞研究已逐步從探索基礎機制轉向臨床轉化研究。尤其在2020年以后,“細胞治療”和“細胞外囊泡”等關鍵詞頻繁出現,表明這些領域已成為當前的研究前沿。
臨床進展:免疫耐受與再生修復的突破
值得關注的是,近年多項臨床研究已初步驗證干細胞策略的可行性與潛力。2025年,梅奧診所領銜的一項III期臨床試驗顯示,MDR-101方案(通過供體造血干細胞誘導免疫混合嵌合體)使多數腎移植受者在移植后成功停用常規免疫抑制藥物,實現功能性免疫耐受。這一突破性進展為干細胞介導的耐受策略提供了迄今最有力的臨床證據。

2025年10月,韓國開展的一項單臂研究納入7例慢性活動性抗體介導排斥反應(cABMR)受者,接受同種異體骨髓來源間充質干細胞輸注(4次,每兩周1次,1×10?cells/kg)。結果顯示,治療后估算腎小球濾過率(eGFR)下降斜率由?16.6%減緩至?2.4%,蛋白尿減少,供體特異性抗體(HLA-DSA)平均熒光強度(MFI)降低,T細胞亞群分析提示免疫調節向保護性方向偏移。該研究首次在cABMR人群中證實MSCs不僅安全,且具備延緩功能惡化的潛力。

2024年12月,日本學者嘗試將自體CD34+細胞經腎動脈分次注射于慢性進行性腎病患者(eGFR15–28 mL/min/1.73m2),結果顯示月eGFR斜率由治療前?1.36±1.1升至治療后+0.22±0.71mL/min/1.73m2/月,腎內阻力指數與剪切波速度亦有顯著改善。盡管樣本量有限,該研究首次證實重復經腎動脈干細胞輸注在進展性腎病中的可行性與功能改善趨勢。

2024年7月,由維也納醫科大學牽頭的一項國際研究探索了一種聯合細胞治療策略:在腎移植同時,向受者輸注來自同一供體的骨髓細胞和自體多克隆調節性T細胞(Tregs)。
該研究證實,這種療法能夠在無需維持性三聯免疫抑制治療的情況下,選擇性清除供體特異性的T細胞克隆,同時保留整體T細胞受體庫的多樣性,從而有效降低針對移植腎臟的免疫反應。相關成果已發表于《柳葉刀》旗下子刊eBioMedicine。這一策略為在器官移植中實現“免疫耐受”提供了新的組合范式。

前景展望:多中心協作與長期隨訪驅動轉化
總體而言,干細胞療法在腎移植領域的研究正穩步推進,臨床試驗數量持續增長,研究重點正從基礎免疫機制向臨床轉化轉移。MDR-101、MSCs治療cABMR、CD34+細胞再生治療及Tregs聯合輸注等代表性研究,初步展示了干細胞在免疫調節與組織修復中的多元應用前景。
然而,當前大多數研究仍處于早期階段,III/IV期試驗匱乏,行業參與度不足,細胞產品標準化與質控體系尚未統一,監管路徑仍待明晰。此外,全球供腎短缺的現實進一步凸顯了開發新型免疫調節策略以提升移植器官長期存活率的緊迫性。
展望未來,亟需推進多中心、隨機對照試驗,建立統一的監管與標準體系,并積累長期隨訪數據,以加速干細胞療法在腎移植領域的臨床轉化與推廣應用。
參考資料:
[1]:https://www.sciencedirect.com/science/article/pii/S1015958426004811?via%3Dihub#bib2
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信