引言:間充質(zhì)干細(xì)胞的獨(dú)特地位
間充質(zhì)干細(xì)胞(Mesenchymal Stem Cells,MSCs)是一類源自成體組織的多潛能干細(xì)胞,最早由Friedenstein等人在上世紀(jì)70年代于骨髓中發(fā)現(xiàn)。此后,科學(xué)界基底在脂肪、牙髓、胎盤、臍帶、甚至羊膜液,滑膜組織中成功分離出相似性質(zhì)的細(xì)胞群。MSCs可更新自我,并在適當(dāng)?shù)臈l件下采集多種細(xì)胞類型,尤其是在再生醫(yī)學(xué)、免疫治療和抗炎研究中表現(xiàn)出非凡潛力。
與干細(xì)胞相比,MSCs不涉及倫理爭(zhēng)議,此外還具有高度免疫相容性和顯著的生物調(diào)節(jié)特性。正因如此,MSCs已成為全球細(xì)胞治療研究中最活躍的細(xì)胞類型之一,據(jù)統(tǒng)計(jì),國(guó)際調(diào)查的相關(guān)臨床試驗(yàn)已超過1,500項(xiàng)。
一、 間充質(zhì)干細(xì)胞的核心修復(fù)機(jī)制
MSCs的治療價(jià)值并非僅僅依靠簡(jiǎn)單的“細(xì)胞替代”,而是通過以下四大協(xié)同作用實(shí)現(xiàn)的:
- 主動(dòng)歸巢(Homing):MSCs像擁有導(dǎo)航系統(tǒng)的“維修工”,能感應(yīng)損傷組織釋放的炎癥信號(hào)(如CXCL12),定向聚集到受損部位。
- 旁分泌效應(yīng)(Paracrine Signaling):MSCs猶如一個(gè)“移動(dòng)制藥廠”,分泌大量的細(xì)胞因子和生長(zhǎng)因子,抑制細(xì)胞凋亡,促進(jìn)血管再生。
- 免疫調(diào)節(jié):在炎癥環(huán)境下,MSCs能將促炎的免疫細(xì)胞轉(zhuǎn)化為抗炎型,平息過度免疫反應(yīng)。
- 微環(huán)境重塑:通過改善損傷部位的營(yíng)養(yǎng)和信號(hào)環(huán)境,激活人體自身的內(nèi)源性修復(fù)潛能。
二、 間充質(zhì)干細(xì)胞(MSCs)的十大領(lǐng)先優(yōu)勢(shì)
1、極高的科研確定性與證據(jù)支撐
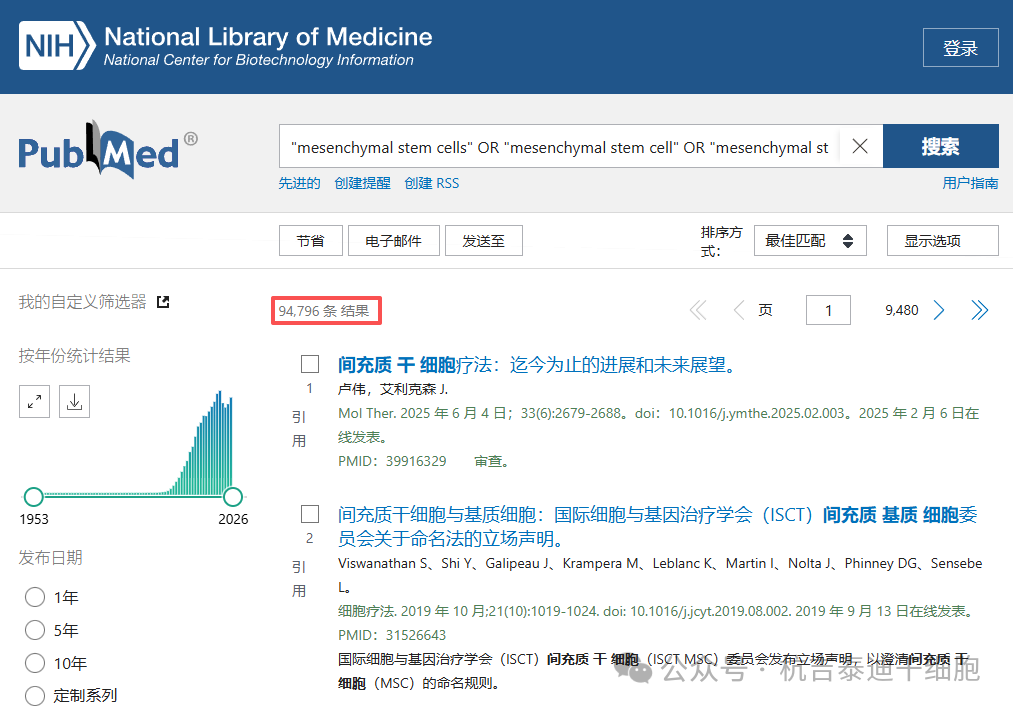
MSCs是研究最為透徹的成體干細(xì)胞之一。目前,關(guān)于其生物學(xué)特性、安全性的全球科學(xué)文獻(xiàn)已有94,796篇。這為臨床轉(zhuǎn)化提供了堅(jiān)實(shí)的循證醫(yī)學(xué)基礎(chǔ)。
2、無(wú)倫理爭(zhēng)議的獲取途徑
MSCs可從成年個(gè)體的骨髓、脂肪,以及新生兒的臍帶、胎盤中提取。這種非侵入性或廢棄物利用的方式,完全符合醫(yī)學(xué)倫理規(guī)范,易于被大眾和法律接受。
3、多向分化潛能(跨胚層修復(fù))
MSCs 具有極強(qiáng)的“塑形”能力。在特定誘導(dǎo)下,它們不僅能分化為骨、軟骨、脂肪、肌腱,甚至展現(xiàn)出跨胚層分化為神經(jīng)細(xì)胞和肝細(xì)胞的潛力,極大擴(kuò)展了治療譜系。
4、成熟的體外標(biāo)準(zhǔn)化培養(yǎng)體系
醫(yī)學(xué)界已掌握了精密的 MSCs 離體分離與純化方案。通過標(biāo)準(zhǔn)化的 GMP 實(shí)驗(yàn)室操作,可以確保細(xì)胞在擴(kuò)增過程中保持高度的純度和活性,實(shí)現(xiàn)高質(zhì)量制備。
5、強(qiáng)大的傳代與倍增能力
MSCs 在體外培養(yǎng)中展現(xiàn)出極強(qiáng)的增殖活力。即使經(jīng)過多次傳代,仍能保持穩(wěn)定的染色體核型和分化潛能,這意味著少量的初始組織即可產(chǎn)生供應(yīng)數(shù)千人次使用的細(xì)胞量。
6、突破性的規(guī)模化生產(chǎn)技術(shù)
借助3D生物反應(yīng)器和微載體技術(shù),結(jié)合對(duì)低氧環(huán)境的精準(zhǔn)模擬,臨床可以實(shí)現(xiàn) MSCs的工業(yè)化規(guī)模擴(kuò)增,徹底解決細(xì)胞數(shù)量不足的瓶頸[1]。
7、動(dòng)態(tài)的旁分泌調(diào)節(jié)功能
MSCs能夠合成并分泌多種大分子物質(zhì),這些物質(zhì)是已知的造血細(xì)胞調(diào)節(jié)因子。它們分泌的外泌體(Exosomes)正成為治療心血管及神經(jīng)系統(tǒng)疾病的新手段[2]。
8、精準(zhǔn)的基因產(chǎn)物遞送載體
利用MSCs天然的“歸巢性”,科學(xué)家可以將其作為載體,通過基因工程手段攜帶抗癌藥物或修復(fù)蛋白,“快遞”至體內(nèi)的特定病灶區(qū)域,實(shí)現(xiàn)精準(zhǔn)靶向治療。
9、卓越的免疫豁免特性
MSCs缺乏啟動(dòng)免疫反應(yīng)所必需的B7家族共刺激分子[3]。這使得MSCs制劑可以在主要組織相容性復(fù)合體(MHC)屏障間進(jìn)行移植,而無(wú)需擔(dān)心免疫排斥反應(yīng)或需要進(jìn)行免疫抑制治療,從而使其成為一種通用的干細(xì)胞來源。
10、完善的商業(yè)化支持體系
目前,全球已形成成熟的MSCs產(chǎn)業(yè)供應(yīng)鏈。從專用培養(yǎng)基到自動(dòng)化檢測(cè)工具,完善的配套設(shè)施極大地縮短了從實(shí)驗(yàn)室研究到病床前應(yīng)用的轉(zhuǎn)化時(shí)間。
三、 不同來源MSCs的臨床選擇建議
為了更精準(zhǔn)地應(yīng)用,我們需要了解不同來源MSCs的特性差異:
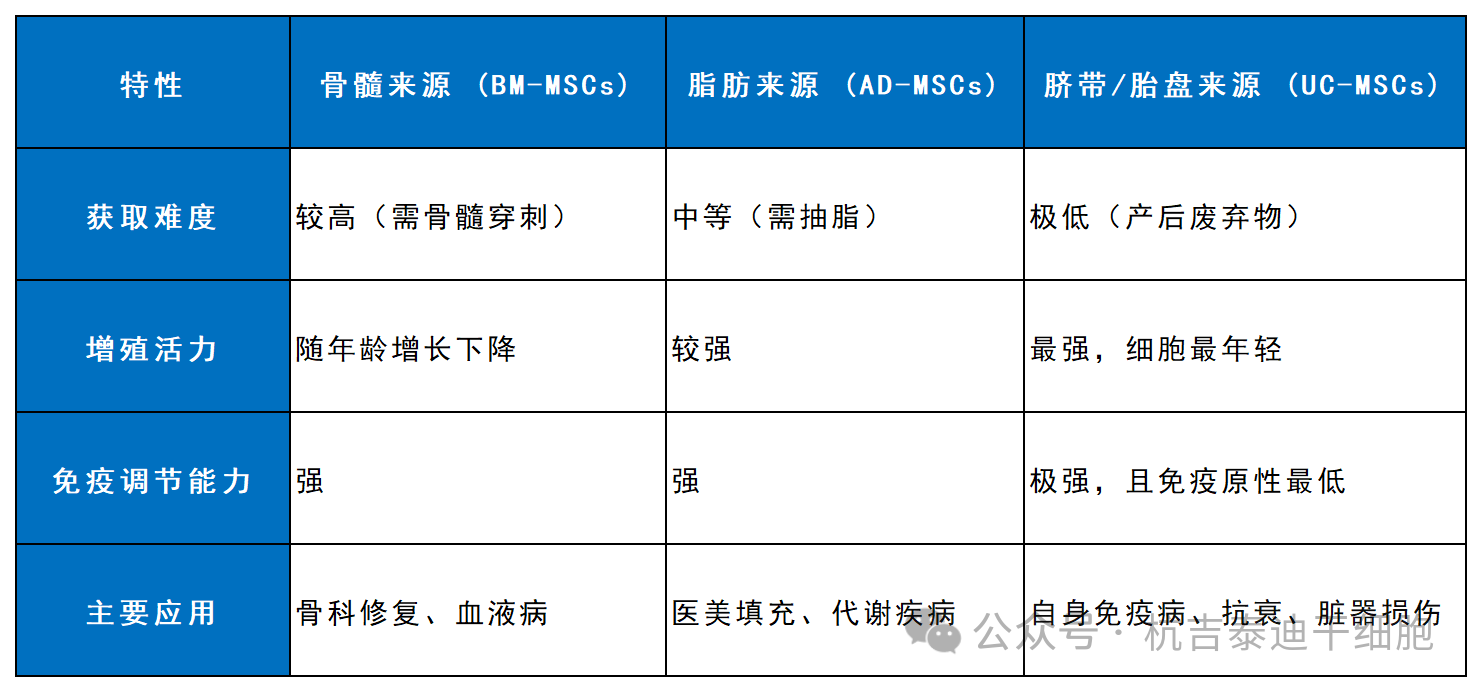
四、 消費(fèi)指南:如何選擇高質(zhì)量干細(xì)胞制劑?
在選擇MSCs制劑時(shí),應(yīng)遵循以下“五看”核心標(biāo)準(zhǔn):
看源頭與合規(guī):首選新生兒圍產(chǎn)期組織(如臍帶)來源。必須附帶《供者知情同意書》并經(jīng)過嚴(yán)格的傳染病篩查。
看實(shí)驗(yàn)室資質(zhì):制備車間必須達(dá)到GMP級(jí)別,并擁有國(guó)家級(jí)備案(如中國(guó)醫(yī)藥生物技術(shù)協(xié)會(huì)備案)或國(guó)際認(rèn)證(如AABB認(rèn)證)。
看核心檢測(cè)報(bào)告:
- 活性:活細(xì)胞比例應(yīng) >90%。
- 純度:CD73/CD90/CD105陽(yáng)性率應(yīng)≥95%。
- 安全性:細(xì)菌、真菌、支原體檢測(cè)必須為陰性,且內(nèi)毒素含量達(dá)標(biāo)。
看有效劑量:高質(zhì)量制劑會(huì)明確標(biāo)注有效細(xì)胞數(shù)量(如5×10^7個(gè)),而非模糊的單位。
看冷鏈與時(shí)效:細(xì)胞必須在2-8°C專業(yè)恒溫箱運(yùn)輸,并明確標(biāo)注出庫(kù)時(shí)間,確保在活性窗口期內(nèi)完成使用。
五、 結(jié)語(yǔ)
間充質(zhì)干細(xì)胞不僅是實(shí)驗(yàn)室里的科學(xué)奇跡,更是臨床醫(yī)學(xué)中真實(shí)存在的“萬(wàn)能鑰匙”。隨著3D生物打印技術(shù)和無(wú)細(xì)胞療法的融合,MSCs將在精準(zhǔn)醫(yī)療和延長(zhǎng)人類健康壽命領(lǐng)域展現(xiàn)出更加驚人的潛力。
參考資料:
[1] Godara P, et al. Mini-review: Design of bioreactors for mesenchymal stem cell tissue engineering. J Chem Technol Biotechnol 2008; 83: 408–420.
[2] Haynesworth S, Reuben D, Caplan A. Cell-based tissue engineering therapies: The influence of whole body physiology. Advanced Drug Delivery Reviews 1998; 33(1-2): 3-14.
[3] Tipnis S, Viswanathan C, Majumdar A. Immunosuppressive properties of human umbilical cord-derived mesenchymal stem cells: Role of B7-H1 and IDO. Immunology and Cell Biology 2010; 88: 795-806.免責(zé)說明:本文僅用于傳播科普知識(shí),分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請(qǐng)隨時(shí)聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信