12月1日至4日,美國加利福尼亞州圣地亞哥舉行的第18屆阿爾茨海默病臨床試驗(CTAD)大會上。美國再生生物醫學公司(Regeneration Biomedical, Inc.,簡稱RBI)公布了全球首個用于治療阿爾茨海默病的自體干細胞接腦內注射療法的I期臨床試驗完整結果。[1]
研究顯示,在早期的1期臨床試驗中,7名接受了這種治療的輕中度阿爾茨海默病患者,83%的人認知能力得到改善,同時與疾病相關的腦部“垃圾蛋白”水平也明顯降低。
這一結果,讓長期難以突破的阿爾茨海默病治療領域出現新的曙光。
一、阿爾茨海默病的治療困境
要理解干細胞療法突破的意義,首先需要認識到當前阿爾茨海默病治療所面臨的現實局限。
目前,FDA已批準的與阿爾茨海默病相關的藥物,多屬于靶向淀粉樣蛋白或tau蛋白的抗體類藥物,如 Leqembi和Kisunla。這些藥物的確能夠減少大腦內的淀粉樣斑塊沉積,但在改善患者認知功能方面的成效有限,并且伴隨明顯的安全風險,包括腦腫脹和微出血等嚴重不良事件。[2]
與此同時,全球藥企在該領域的研發進展也不斷遇阻。強生的抗tau抗體項目以及諾和諾德基于GLP-1的阿爾茨海默病研究均未能證明明確的臨床獲益,這進一步凸顯了行業對于全新治療機制的迫切需求。
也正是在這樣的背景下,干細胞療法提出了一條與傳統截然不同的思路——不再單純關注“清除病理蛋白”,而是嘗試激活大腦自身的修復潛能,推動神經再生。
二、什么是“干細胞直接腦內注射”?和其他干細胞治療有什么區別?
RBI公司開發的干細胞直接入腦療法名為RB-ADSC,其核心是一種自體Wnt富集干細胞療法。聽起來復雜,其實原理很直接:從患者腹部抽取約50毫升脂肪,從中提取并培養患者自己的干細胞。
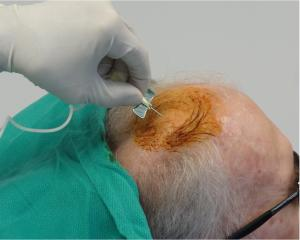
這些細胞經過特殊處理后,能高表達一種叫做“Wnt”的關鍵信號分子,這種分子與喚醒大腦內沉睡的干細胞有關。準備好細胞后,通過一個植入頭皮下的小型儲液裝置,將細胞直接輸送到充滿腦脊液的腦室系統中。
“我們的療法利用富含Wnt表達的自體干細胞,旨在刺激休眠的腦室干細胞群,”RBI創始人、神經外科醫生克里斯托弗·杜馬博士解釋道。
與其他干細胞治療有何不同?
| 傳統干細胞治療(靜脈 / 鞘內注射) | RBI 干細胞直接腦內注射(RB-ADSC) |
|---|---|
| 干細胞進入血液后分布在全身,僅有極少部分能到達大腦 | 直接進入腦室系統,作用靶點更精準 |
| 治療機制多為抗炎、改善微環境 | 激活沉睡的神經干細胞、促進再生 |
| 效果往往局限于改善癥狀與炎癥 | 目標在于重建神經網絡、改善認知功能 |
| 多用于中風后遺癥、腦損傷等 | 首次針對阿爾茨海默病明確設計的入腦療法 |
三、Ⅰ期臨床成果:83%患者認知能力得到顯著改善
在已完成的第一階段試驗中,共有9名患者參與,其中7名的數據在CTAD大會上公布。這些患者年齡均在80歲以下,處于阿爾茨海默病的中期階段。
治療過程分三步:首先從患者腹部抽取少量脂肪;其次通過簡單手術在頭皮下植入一個小型儲液裝置;最后將準備好的干細胞注入大腦。整個過程耐受性良好,主要不良反應僅為抽脂部位的輕微不適和切口疼痛。
結果顯示:
安全性良好: 治療總體耐受性良好,主要不良反應僅限脂肪抽取部位的輕微不適和植入部位的短暫疼痛。在干細胞被注入大腦后,長達25周的觀察期內,未報告任何與該步驟直接相關的不良事件。
生物標志物改善:83%的患者腦脊液中有害的磷酸化tau蛋白水平下降;66%的患者大腦中的淀粉樣蛋白沉積在PET影像上呈現減少趨勢。
關鍵認知指標提升: 最令人鼓舞的是,83%的患者在阿爾茨海默病評估量表認知子量表上的得分出現改善,中位數得分從基線的53分下降到治療12周后的38分(分值越低表示認知功能越好)。

這一系列結果讓科學家們看到了真正改善認知功能的可能——這是現有藥物無法做到的。
四、未來之路,二期試驗啟動,驗證療效的關鍵一步
基于一期試驗的積極數據,美國FDA已批準開展二期臨床試驗。
這項研究計劃招募約115名患者,采用隨機、雙盲、安慰劑對照的嚴謹設計,旨在進一步評估療法的安全性和有效性。患者將接受不同劑量的干細胞治療或安慰劑。
除了繼續監測認知功能變化,研究還將通過腦脊液檢測、腦部MRI和PET成像等多種手段,全面評估療法對大腦的影響。
“進入二期試驗,標志著我們向開發一種能夠恢復神經功能的再生療法邁出了關鍵一步。”再生生物醫學公司首席執行官比爾·米勒表示。
五、對于患者和家屬:該如何看待這條新路?
對于正在與阿爾茨海默病抗爭的家庭而言,每一個新的研究進展都意味著希望。然而,面對早期研究,我們更需要理性看待它的位置與意義。
1. 它不是“最后一根救命稻草”,但確實是一個新的認真選項
從已經公布的一期臨床試驗結果來看,無論是自體干細胞直接進入大腦腦室,還是其他在研的間充質干細胞或神經干細胞方向,都有一部分患者的認知能力、情緒狀態或生活能力出現了改善;腦脊液和影像標志物也在往更健康的方向走。
對于那些:
- 已經規律使用現有藥物(如抗淀粉樣蛋白、膽堿酯酶抑制劑);
- 但病情仍在逐漸進展;
- 家屬長期處于焦慮、無力與希望之間拉扯的患者家庭;
干細胞療法至少提供了一個新的信號:“還有人在向前探索,而且已經有人在真實世界看到了初步的積極變化。”
2. 它代表一種“從控制衰退到激活修復”的全新治療范式
目前AD治療的主流路線仍以延緩退化、減少有害物質為核心。而干細胞路線的共同目標是:
- 不只是盯著記憶下降分數本身;
- 更關注大腦整體修復機制、神經網絡穩定性、炎癥狀態、突觸功能與生活能力。
這意味著,如果研究繼續獲得成功,未來阿爾茨海默病的治療圖景,有可能變成這樣:
- 一端,是現在已經成熟的藥物和認知干預,負責盡量減緩衰退;
- 另一端,是干細胞、外泌體等“修復型工具”,幫助大腦重建更健康的神經網絡;
- 中間,是更加精細的影像、生物標志物和功能評估,實現長期管理與個體化治療。
對于患者來說,這不再只是“能不能再加一種藥”的問題,而是有機會多一個真正朝著修復方向努力的新工具。
3. 它在提醒我們:阿爾茨海默病不是完全不可逆的,大腦仍然有“恢復窗口”
干細胞研究給出的一個重要啟發是:大腦不是靜止的,即便進入退行性階段,也仍然存在被激活、被修復、被重建的可能性。
在合適的時間窗口、合適的方式使用合適的細胞幫助大腦:
- 可能不僅能減慢退化;
- 還能讓記憶、語言、行動能力、情緒等慢慢向更好的地方挪動一點。
對于已經在阿爾茨海默病中堅持了很久的家庭來說,這句話本身就是一種力量——我們努力守住當下的生活,同時,還有人在為“可能更好的一天”開路。
結語
阿爾茨海默病的治療探索,正在經歷一場從“治標”到試圖“治本”的深刻轉變。干細胞直接腦內注射療法,正是這一轉變中的前沿代表。
盡管前路依然漫長,二期、三期試驗的重重驗證仍在后方,但一期試驗點燃的這簇“改善”之火,已足夠照亮新的方向——那就是不再僅僅滿足于讓衰退慢一點,而是勇敢探索讓功能好一點的可能。對于在漫長病程中堅守的患者與家庭,這份來自科學前沿的、務實的希望,或許正是堅持下去的重要力量之一。
參考資料:
[1]https://fox59.com/business/press-releases/ein-presswire/871494470/rbi-inc-to-present-their-phase-1-first-in-human-direct-to-brain-autologous-stem-cell-therapy-results-at-ctad-2025/
[2]https://apnews.com/press-release/ein-presswire-newsmatics/exclusive-safe-direct-to-brain-autologous-stem-cell-therapy-shows-promise-in-alzheimers-03607a5b073acbbff29a6e18ca7841cd
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信