當(dāng)我們的身體受傷時,某些部位的恢復(fù)能力令人驚嘆。例如,角膜上的輕微擦傷可能在一天內(nèi)愈合。然而,大腦卻并非如此。成年的腦細(xì)胞通常極其穩(wěn)定,卻也因此難以再生,一旦遭遇中風(fēng)等嚴(yán)重?fù)p傷,其復(fù)雜的神經(jīng)回路便會中斷,功能隨之喪失。
科學(xué)家一直致力于利用干細(xì)胞療法來修復(fù)受損大腦,但挑戰(zhàn)重重。移植后的細(xì)胞不僅要能在損傷造成的惡劣“炎癥沼澤”中存活,還要能夠穿越疤痕組織構(gòu)成的屏障,精準(zhǔn)地整合到現(xiàn)有的神經(jīng)回路中,才能真正恢復(fù)功能。
2026年1月8日,《細(xì)胞干細(xì)胞》期刊發(fā)表了一項(xiàng)突破性研究。由桑福德·伯納姆·普雷比斯醫(yī)學(xué)發(fā)現(xiàn)研究所和杜克-國大醫(yī)學(xué)院聯(lián)合開展的研究表明,將特定的人類干細(xì)胞移植至中風(fēng)小鼠模型后,這些細(xì)胞不僅成功存活、成熟為神經(jīng)元,更令人振奮的是,它們能像擁有內(nèi)置“GPS”一樣,主動導(dǎo)航,跨越損傷區(qū)域,與宿主大腦的特定區(qū)域建立正確的功能性連接,從而恢復(fù)失去的神經(jīng)功能[1]。

“治療中風(fēng)損傷,就像試圖在充滿威脅的沼澤中修橋,”該研究的領(lǐng)導(dǎo)者、張素春博士解釋道。“關(guān)鍵在于,我們不能只是繞開這片沼澤,而是要讓新細(xì)胞在其中扎根,并重建橋梁。”
研究團(tuán)隊(duì)利用小分子和蛋白質(zhì)的混合“支持系統(tǒng)”,成功幫助移植細(xì)胞在中風(fēng)形成的空腔中存活并生長。隨后,他們借助三維重建和基因條形碼追蹤等尖端技術(shù),深入觀察了這些新生神經(jīng)元的“行為”。
他們發(fā)現(xiàn),移植后發(fā)育出的不同亞型神經(jīng)元,其延伸出軸突(負(fù)責(zé)信號傳遞的“長導(dǎo)線”)的模式,與健康大腦皮層和脊髓中的同類神經(jīng)元高度相似。
更重要的是,通過單細(xì)胞測序分析,研究人員揭示了一個核心機(jī)制:每一種神經(jīng)元亞型都攜帶一套獨(dú)特的“內(nèi)在分子代碼”(由特定基因和轉(zhuǎn)錄因子構(gòu)成)。這套代碼在細(xì)胞成熟為神經(jīng)元后自動激活,精確地指導(dǎo)其軸突向大腦或脊髓的特定目標(biāo)區(qū)域生長,從而與正確的“伙伴”建立連接。
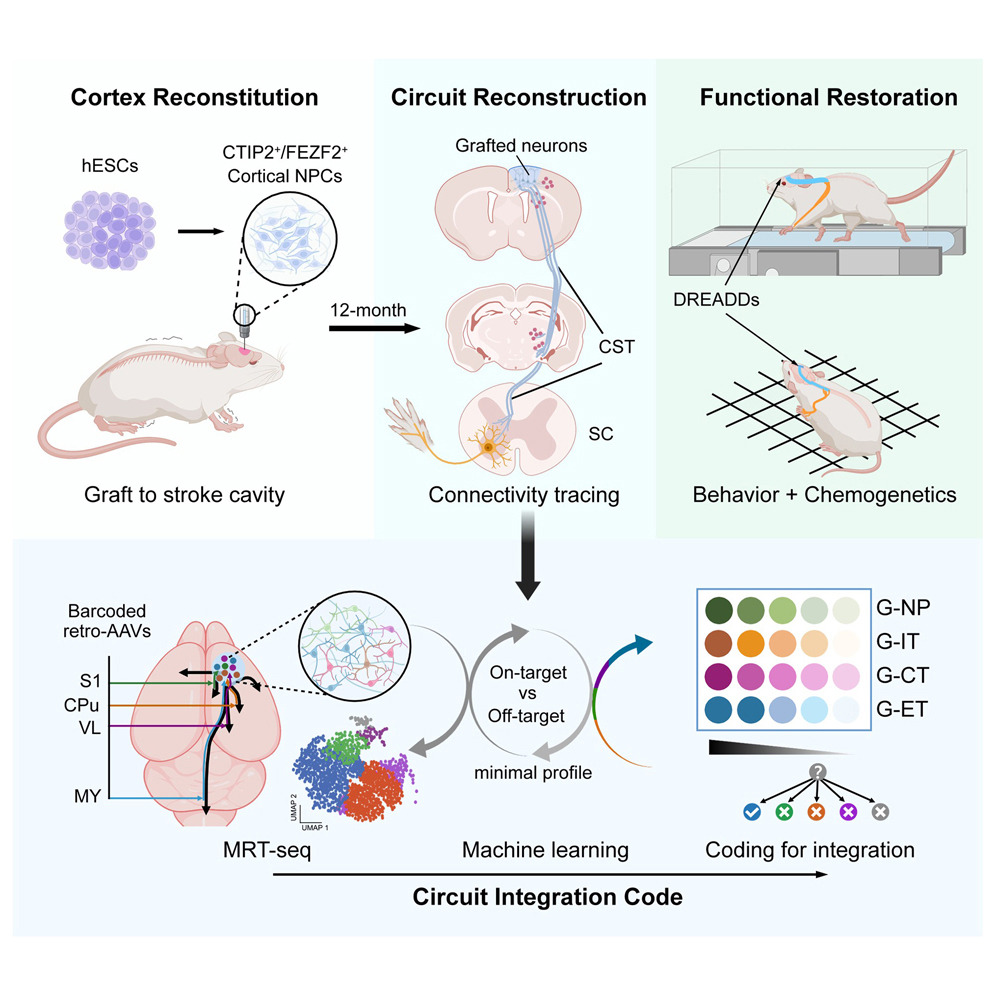
為了驗(yàn)證這一機(jī)制,研究團(tuán)隊(duì)對干細(xì)胞進(jìn)行了基因改造,敲除了一種名為Ctip2的關(guān)鍵轉(zhuǎn)錄因子。結(jié)果,這些細(xì)胞的軸突投射模式發(fā)生了顯著改變,錯誤地嘗試連接海馬體和杏仁核等區(qū)域。這直接證明了內(nèi)在的基因程序?qū)B接特異性起著決定性作用。
一、 移植的神經(jīng)干細(xì)胞如何在腦內(nèi)建立連接?
本研究揭示了兩個關(guān)鍵步驟:
環(huán)境支持與存活:首先,通過生化支持手段(小分子藥物和結(jié)構(gòu)蛋白),為移植到惡劣損傷環(huán)境(炎癥、疤痕)中的干細(xì)胞創(chuàng)造生存條件,使其能夠存活并分化為神經(jīng)元。
內(nèi)在編碼的精準(zhǔn)導(dǎo)航:這是最核心的發(fā)現(xiàn)。移植干細(xì)胞在分化為不同亞型的神經(jīng)元后,并非隨機(jī)生長。每種亞型都繼承或激活了一套預(yù)設(shè)的“分子導(dǎo)航指令”(即特定的基因表達(dá)譜和轉(zhuǎn)錄因子,如Ctip2)。這套“內(nèi)在代碼”如同施工藍(lán)圖,精確引導(dǎo)新生神經(jīng)元的軸突,穿越復(fù)雜環(huán)境,定向生長至其預(yù)設(shè)的、功能匹配的宿主腦區(qū)(如皮層、脊髓的特定核團(tuán)),并與之形成具有功能的突觸連接,從而重建被破壞的神經(jīng)回路。
二、 這項(xiàng)研究意味著什么?
這項(xiàng)研究的科學(xué)意義和臨床前景極為重大:
原理性突破:首次系統(tǒng)性地揭示了移植神經(jīng)元的“內(nèi)在導(dǎo)航代碼”機(jī)制,證明了即使在成年的受損大腦復(fù)雜環(huán)境中,正確類型的神經(jīng)元仍能“記住”自己的使命和目標(biāo)地址。這解決了細(xì)胞療法中“整合精準(zhǔn)性”的核心難題。
從“盲目移植”到“精準(zhǔn)設(shè)計(jì)”:研究意味著未來可以根據(jù)損傷部位和所需修復(fù)的回路,預(yù)先選擇或體外定向誘導(dǎo)出具有特定“導(dǎo)航代碼”的神經(jīng)元亞型進(jìn)行移植。例如,針對運(yùn)動通路損傷,就移植高表達(dá)特定引導(dǎo)基因的運(yùn)動皮層神經(jīng)元亞型。
提升治療可預(yù)測性與療效:通過操控像Ctip2這樣的關(guān)鍵轉(zhuǎn)錄因子,理論上可以微調(diào)移植神經(jīng)元的連接偏好。這極大增強(qiáng)了細(xì)胞療法的可預(yù)測性和可控性,為“量身定制”修復(fù)方案奠定了基礎(chǔ),有望顯著提高功能恢復(fù)的效果。
帶來廣闊的應(yīng)用希望:這一發(fā)現(xiàn)不僅適用于中風(fēng),也為治療脊髓損傷、帕金森病、阿爾茨海默病等其他因神經(jīng)連接中斷或丟失導(dǎo)致的神經(jīng)系統(tǒng)疾病,提供了全新的策略和堅(jiān)實(shí)的理論依據(jù)。它標(biāo)志著再生醫(yī)學(xué)在修復(fù)大腦功能方面,從“可能替代細(xì)胞”邁向了“可能精準(zhǔn)重建連接”的新階段。
總之,這項(xiàng)研究如同發(fā)現(xiàn)了修復(fù)大腦線路的“接線手冊”,為開發(fā)下一代高效、精準(zhǔn)的神經(jīng)再生療法照亮了道路,給全球數(shù)以百萬計(jì)的相關(guān)疾病患者帶來了新的希望。
參考資料:
[1]:https://www.cell.com/cell-stem-cell/abstract/S1934-5909(25)00442-4
免責(zé)說明:本文僅用于傳播科普知識,分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請隨時聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信