類風濕性關節炎 (RA) 是一種高度流行的慢性進行性自身免疫性疾病,主要影響關節和肌肉。相關的炎癥、疼痛和運動受限會對患者的生活質量 (QOL) 產生負面影響,甚至可能導致過早死亡。此外,諸如抗炎藥物之類的常規治療僅是對癥治療。
近日,琉球大學醫學研究生院整形與重建外科在國際醫學期刊《細胞》上發表了一篇《間充質干細胞治療類風濕關節炎的可能性和挑戰》的綜述,這篇綜述描述了間充質干細胞療法在治療類風濕關節炎的現狀以及更廣泛的臨床應用的機遇和挑戰。
什么是類風濕關節炎,類風濕關節炎的發病原因
類風濕性關節炎(RA)是一種慢性全身性自身免疫性疾病,其典型特征是滑膜炎癥、軟骨和骨破壞以及進行性關節畸形。它與骨關節炎在病因、病程、癥狀特征、典型的身體部位和臨床治療等方面都有所不同。進行性RA患者更容易過早死亡(75歲之前),主要死于心血管和肺部疾病。疾病早期主要影響滑膜關節,但最終會擴散到肺部、血管和身體其他部位。此外,RA是最常見的自身免疫性疾病之一,2002年全球發病率估計為0.5-1.0%。女性發病率高于男性(4:1),發病高峰期在40至60歲之間。因此,RA嚴重降低長期生活質量(QOL),尤其是女性患者,需要長期的臨床治療。
越來越多的證據表明,顯性RA的病因病理涉及先天性和適應性免疫系統功能障礙導致的慢性炎癥,包括對自身抗原的免疫反應、細胞因子信號網絡異常以及免疫復合物的補體激活。最近的報道表明,疾病其他階段(如早期和難治性階段)的病理過程可能并非完全由免疫功能失調引起。相反,早期RA很可能是由抗瓜氨酸蛋白抗體(ACPA)通過白細胞介素(IL)/T輔助細胞(Th)細胞因子途徑觸發的,而難治性RA更可能是由于細胞自主遺傳和表觀遺傳擾亂,涉及慢性炎癥后滑膜細胞中轉化的細胞死亡途徑(見圖1)。
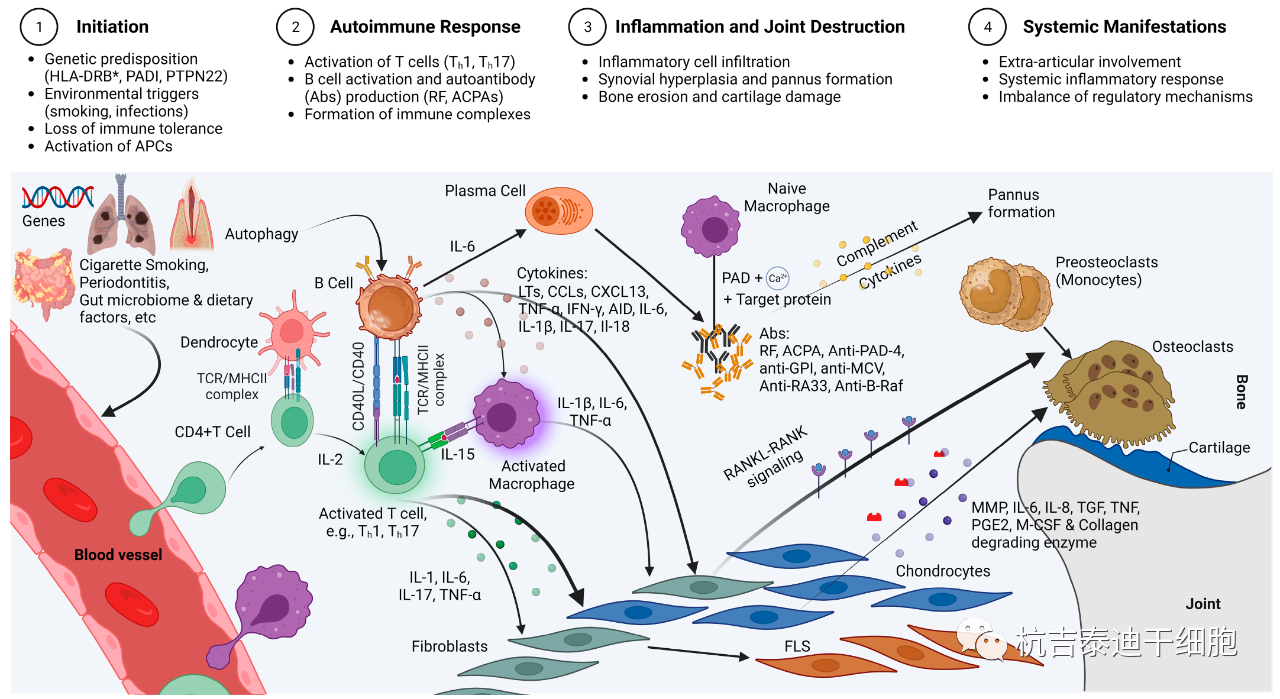
在闡明明顯的RA病因病理學方面已經取得了實質性進展,特別是先天性和適應性免疫系統功能障礙對慢性炎癥的影響。盡管發病和進展的確切機制仍然難以捉摸,但新藥物靶點的發現、早期診斷和新的靶向治療已大大改善了RA患者的預后和生活質量。然而,相當一部分患者出現嚴重的不良反應,表現出較差的反應,或不能耐受長期使用這些藥物,需要更有效和更安全的治療替代方案。越來越多的臨床前和臨床證據表明,間充質干細胞移植是控制慢性炎癥和促進包括RA在內的難治性疾病患者組織再生的安全有效的治療策略。
間充質干細胞恢復健康的能力
間充質干細胞是一種多能成人或體細胞干細胞群,長期以來一直用于臨床前研究,最近各種間充質干細胞在臨床試驗中顯示出前景。
間充質干細胞避免了與獲取人類ESCs相關的倫理問題,而且可以從患者身上獲取,用于個性化治療。此外,這些細胞可分化成中胚層來源的多種細胞類型,包括骨細胞、軟骨細胞、心肌細胞和脂肪細胞,因此在治療某些骨關節疾病(如RA)時,它們可能是iPSCs的一種同樣可行的替代品。此外,間充質干細胞還具有其他臨床應用的理想特性,包括低免疫原性、強免疫調節能力以及抗炎、促血管生成和抗細胞凋亡活性。此外,間充質干細胞治療還具有成本效益,因為這些細胞可根據最終應用的不同從多種組織中提取。由于不同來源的間充質干細胞具有不同的分化潛能譜,因此特定組織是治療RA的首選(表1)。
表1:來自四種常見來源組織的MSC的特性,用于治療關節炎疾病。

間充質干細胞的免疫調節和抗炎能力對于有效治療自身免疫性疾病和慢性炎癥性疾病至關重要。
間充質干細胞治療類風濕關節炎的機制
MSC的愈合特性直接受到組織微環境中炎癥水平的影響(表2),這表明免疫細胞功能是MSC的主要治療靶點。潛在的治療機制包括EV和其他可溶性因子的旁分泌活性,以及通過細胞與細胞接觸的直接調節。
表2:炎癥微環境對MSC免疫調節潛力的影響。

間充質干細胞治療類風濕關節炎的優點
使用MSC進行基于細胞的RA治療引起了人們的濃厚興趣,因為這些細胞具有調節多種基本細胞功能的能力,并且由于MHCI類表達極少以及缺乏MHCII類和共刺激分子CD40、CD80和CD86而導致固有的低免疫原性。因此,臨床研究的數量在過去十年中增加了大約四倍,盡管只有不到10%是III期或IV期試驗。
間充質干細胞治療類風濕關節炎的臨床試驗
通過搜索各種試驗注冊中心和互聯網站點,發現了幾項基于MSC的 RA 療法臨床試驗(表3)。其中,UC-MSC是最常見的細胞類型,其次是 AD-MSC和BM-MSC。最多的試驗是在美國進行的,其次是中國、韓國和歐盟。其余的研究是在伊朗、約旦和巴拿馬進行的。早期試驗(I期和II期)占總數的80%以上。
2010年,在韓國的一項試點試驗(2010年)招募了10名自身免疫性疾病患者,其中4名患有RA。自體AD-MSC經擴增可多次輸注,每位患者的劑量范圍為2×108至3.5×108個細胞。該試驗觀察到了臨床益處,一個月內安全施用了多達8×108個細胞。
2012年,在中國的另一項試驗中,四名RA患者通過靜脈 (IV) 輸注接受同種異體MSC。盡管沒有達到緩解,但三名患者在幾個月內表現出中等反應。
2017年,西班牙的一項隨機試驗 (NCT01663116) 涉及53名難治性RA患者,他們接受了不同劑量的同種異體擴增ADMSC (eASC)。經過6個月的監測,觀察到了有希望的結果。RA患者靜脈輸注Cx611耐受性良好,無劑量相關毒性。與安慰劑組相比,觀察到基于EULAR標準、DAS28-ESR和CRP的陽性反應長達三個月。然而,RA患者的難治性特征可能限制了MSC治療的有益效果。該試驗沒有觀察到T細胞群的顯著變化或不良臨床后果,但19%的患者產生了MSC特異性抗HLA-I抗體。
2018年,Kang Stem Biotech資助了韓國的兩項試驗(CURE-IV和FURESTEM-RA)。這些試驗涉及接受同種異體UCB-MSC的初治RA患者。I期試驗 (NCT02221258) 顯示沒有嚴重的不良事件、疾病活動指標的改善以及炎癥細胞因子水平的降低。然而,局限性包括樣本量小和隨訪時間短。一項為期5年的觀察性研究正在進行中,一項I/IIa期隨機雙盲安慰劑對照試驗 (NCT03618784) 目前正在進行中。
2018年,在中國大坪醫院,53名難治性RA患者接受了單劑量靜脈注射異體UC-間充質干細胞(ChiCTR-ONC-16008770)。治療過程中未出現嚴重急性不良反應,臨床安全性和有效性均得到證實。與對照組相比,約54%的間充質干細胞治療患者出現了良好或中度反應,46%的患者沒有臨床反應。觀察到了短暫的療效,建議繼續輸注間充質干細胞以獲得持續療效。血清IFN-γ水平與臨床療效相關,可作為一種預測性生物標志物。
2019年,在中國人民解放軍空軍醫院,172名RA患者接受了單次靜脈注射同種異體UC-MSC(NCT01547091)。未報告嚴重不良反應,根據ACR標準、DAS-28、ESR、HAQ和炎癥標志物減少觀察到顯著緩解。與對照組相比,在短期(長達8個月)和長期(長達3年)中觀察到了有益效果。
表3.全球范圍內針對RA進行的細胞療法的臨床研究。
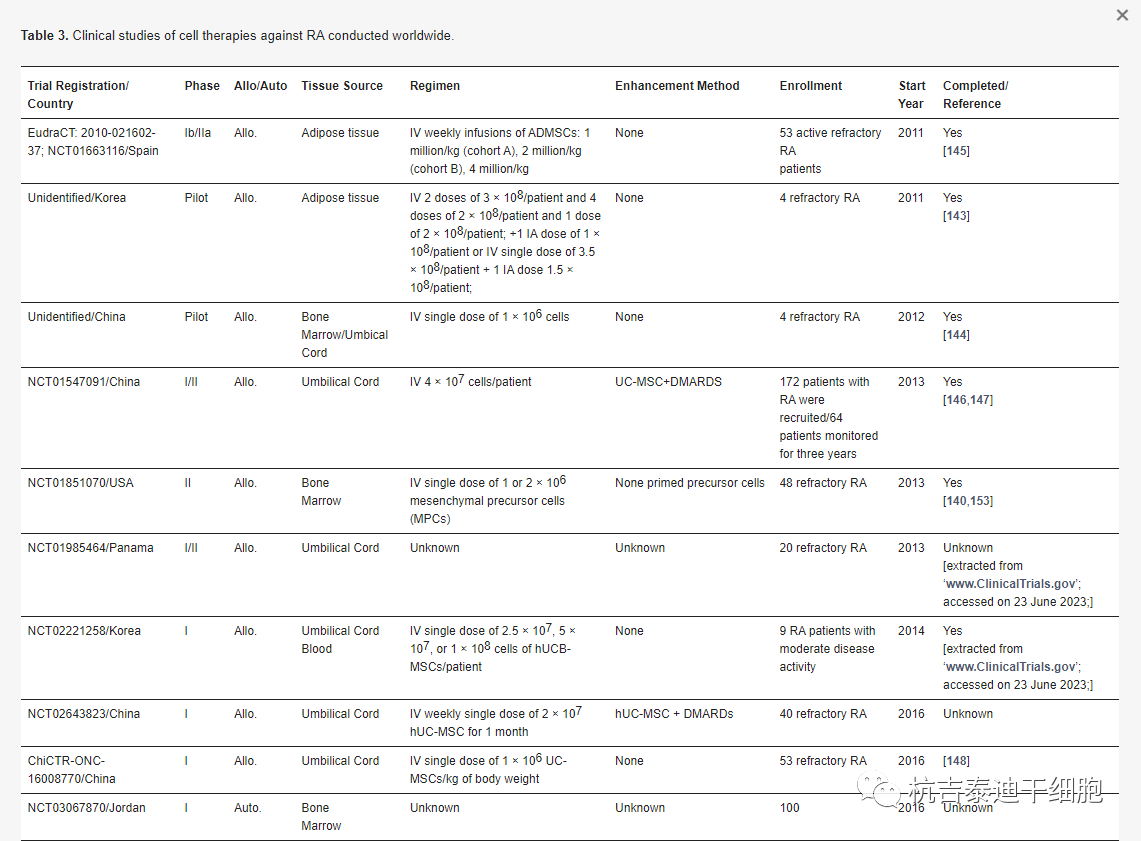
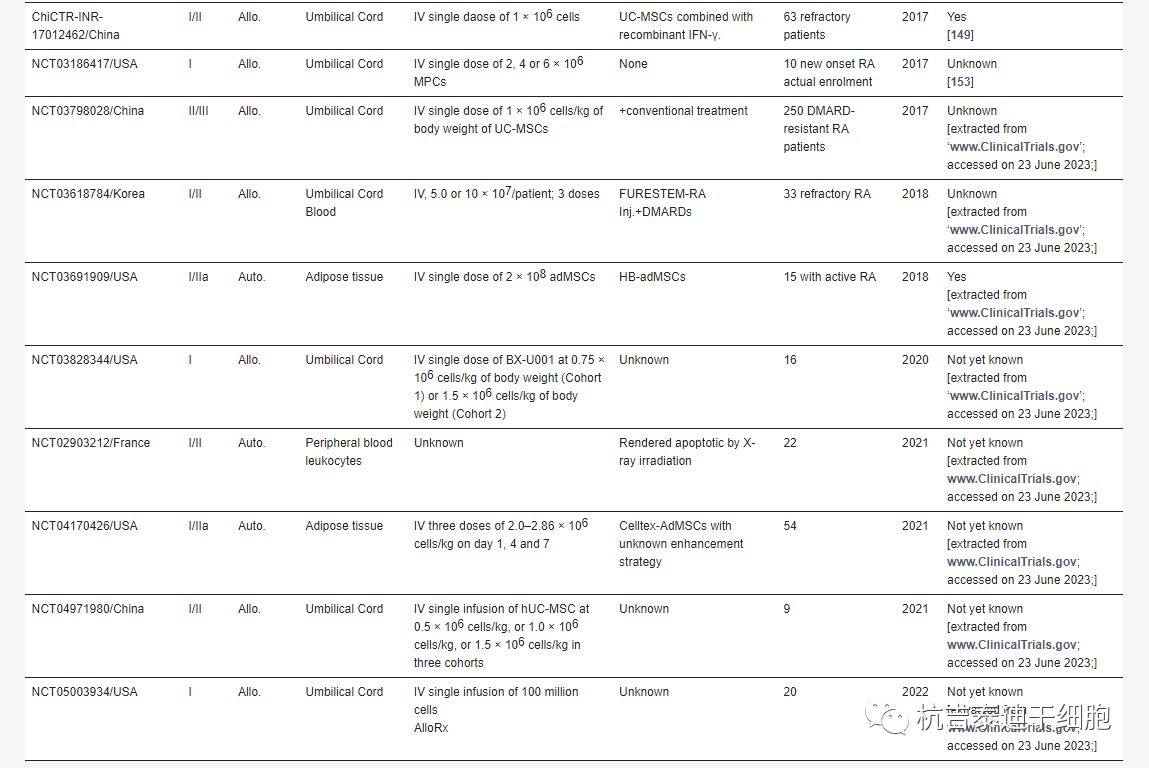
Allo,同種異體;自體的,自體的;ChiCTR-INR,中國登記處,“ www.Chictr.org ”;訪問日期:2023年6月23日;EudraCT,歐盟藥物監管機構臨床試驗數據庫;IA,關節內;IV,靜脈注射;MPC,多能祖細胞;NCT,國家臨床試驗;UC,臍帶
目前,基于間充質干細胞治療RA的幾項臨床試驗正在進行中,每項試驗都有不同的MHC背景、組織來源和細胞劑量。這些試驗包括異體和自體兩種方法,其中臍帶組織是最常見的來源。
這些正在進行的試驗包括巴拿馬干細胞研究所(NCT01985464)Wang等人的一項研究,該研究使用異體UC間充質干細胞治療20名DMARD抗性RA患者。該試驗旨在評估一年后的不良反應、生物學療效和免疫學參數。
另一項試驗(NCT03067870)由約旦的阿拉伯干細胞組織贊助,于2016年啟動,旨在評估自體BM-間充質干細胞治療RA患者的安全性和療效。該研究計劃招募100名患者,使用一個月的VAS評分和六個月的WOMAC評分及影像學檢查監測系統療效,以評估關節再生潛力。
中國西京醫院的一項多中心試驗(NCT03798028)于2019年1月啟動,招募患有中度或重度RA以及貧血和/或間質性肺病的成年RA患者。該試驗旨在評估異體UCB間充質干細胞24周的安全性和療效。
2017年,美國俄亥俄州克利夫蘭MetroHealth醫學中心開始了一項概念驗證I期試驗(NCT03186417)。該研究旨在招募20名新診斷的RA患者,使用患者報告結果測量信息系統計算機適應性測試(PROMIS CAT)、患者指數數據常規評估3(RAPID3)問卷和DAS28-CRP,評估異體BM-MSCs24個月的安全性和有效性。
2018年,Kang Stem Biotech Co.Ltd.在韓國啟動了一項I/IIa期RA試驗(NCT03618784),以評估靜脈注射異體UC-MSCs對33名難治或不耐受RA患者的療效。該研究使用各種評分系統和細胞因子水平分析對患者進行為期16周的監測。
美國德克薩斯州的Hope Biosciences自2018年以來一直在進行一項I/II期試驗(NCT03691909),以評估自體ADMSCs在RA患者中的安全性和有效性。該試驗正在評估長達12個月的多種因素。
美國加利福尼亞州的Baylx公司最近啟動了一項I期試驗(NCT03828344),以評估異體UC-MSCs在難治性RA患者中的安全性和效果。該試驗評估多個標準,預計將于2022年9月完成。
最后,位于美國德克薩斯州休斯敦的Celltex Therapeutics公司目前正在進行一項I/IIa期試驗(NCT04170426),招募患者使用自體 ADMSCs治療DMARD難治性RA患者。該試驗預計于2023年12月完成。
加強基于間充質干細胞治療類風濕關節炎的挑戰與策略
間充質干細胞是治療包括RA在內的多種疾病的一種很有前景的方法。然而,要優化基于間充質干細胞的療法,還需要應對一些挑戰。這些挑戰來自多種因素,如間充質干細胞的來源組織、供體性別、年齡、健康狀況和/或病史,以及組織的處理、培養條件、細胞的冷凍和解凍以及給藥途徑。這些因素極大地影響了間充質干細胞療法的效果,亟待優化。
首先,供體的健康狀況會影響所獲間葉干細胞的各個方面,包括其數量、質量、再生潛力、免疫調節能力和分泌組,因為年齡、炎癥/代謝狀態、藥物/治療和感染性疾病等因素會改變間充質干細胞的特性,從而導致間葉干細胞在表面標志物、分化能力和生理功能方面存在顯著的異質性。為了提高遷移率,人們對表達特定趨化因子受體的間充質干細胞進行了基因改造,而輸送途徑的選擇也會影響其歸巢和旁分泌功能。
另一個挑戰是間充質干細胞的擴增能力有限,因此難以獲得足夠數量的細胞用于臨床試驗。延長培養時間和增加傳代次數會導致增殖減少、形態改變和活力受損。因此,優化培養條件和開發可擴展的生產工藝對克服這一限制至關重要。
與特定間充質干細胞組織來源(如UCB-間充質干細胞)相關的安全問題也需要解決。染色體異常和潛在致瘤性已有報道,因此必須努力確保基于間充質干細胞療法的安全性。從UCB間充質干細胞中克隆單個細胞和使用特異性抗原進行細胞分離的方法已得到探索,但普遍接受的培養方案尚未確定。遵守GMP至關重要,使用生物反應器和自動化系統可為大規模生產提供受控環境和更高的可擴展性。此外,目前正在開發冷凍保存技術,以提高細胞的長期存活率,并方便儲存和運輸。
為了優化間充質干細胞療法,人們研究了各種策略。生物材料策略旨在改善間充質干細胞的功能,但可能會引發免疫反應。間充質干細胞衍生的EVs已在臨床試驗中顯示出前景,人工智能(AI)和工程化EVs領域為推動間充質干細胞治療提供了令人興奮的前景。人工智能可加速藥物開發并提高對間葉干細胞療法的認識,而工程化的間葉干細胞-EVs則可進行修飾以提高治療潛力。
就RA而言,已探索出多種策略來增強間充質干細胞的治療效果。這些策略包括共培養方法、生長因子、細胞因子、受體激動劑、缺氧、自噬和基因修飾。針對免疫受體激動劑(如 TLR3和TLR4)的研究顯示,細胞特性和免疫調節功能均有所改善。用咖啡因預處理間充質干細胞可減少促炎細胞因子的產生并改善疾病狀態。缺氧和自噬條件已顯示出在增加間充質干細胞的免疫功能方面的應用前景。
總結
主要在過去十年中進行的大量研究為基于間充質干細胞的RA療法的有效性和安全性提供了令人鼓舞的證據。
總的來說,間充質干細胞(MSCs)治療類風濕性關節炎(RA)的機制在于兩點:1)免疫調節。抑制免疫反應,消除炎癥,促進Treg細胞恢復到正常水平,從而維持免疫的平衡;2)組織修復。在免疫調節的基礎上,促進軟骨細胞和成骨細胞的增殖,抑制破骨細胞的活性,從而促進軟骨再生和破損骨組織的修復。
已經破壞和變形了的關節,干細胞也不能讓它恢復原來健康的模樣,但是干細胞在改善疼痛和阻斷惡化方面效果顯著。
相信在生物醫療技術的推動下,干細胞終將突破種種難關,克服類風濕關節炎,為廣大患者群體帶來福音。
參考資料:Shimizu Y, Ntege EH, Azuma C, Uehara F, Toma T, Higa K, Yabiku H, Matsuura N, Inoue Y, Sunami H. Management of Rheumatoid Arthritis: Possibilities and Challenges of Mesenchymal Stromal/Stem Cell-Based Therapies. Cells. 2023; 12(14):1905. https://doi.org/10.3390/cells12141905。
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信