本文聚焦于干細胞在修復(fù)1型糖尿病過程中的3大核心作用機制。從分子層面的調(diào)控到胰島微環(huán)境的重塑,逐層解析干細胞如何通過細胞替代、免疫調(diào)節(jié)和微環(huán)境修復(fù)等多重途徑,協(xié)同實現(xiàn)對1型糖尿病癥狀的干預(yù)與改善。

重磅解讀:干細胞如何修復(fù)1型糖尿病?3大核心作用機制全解析
1型糖尿病治療的核心難題與修復(fù)需求
1型糖尿病是一種典型的自身免疫性疾病,其根本問題在于免疫系統(tǒng)“認錯敵人”,錯誤地攻擊并摧毀胰腺中的胰島β細胞。這些β細胞是體內(nèi)唯一能夠分泌胰島素的功能單元,一旦遭到大規(guī)模破壞,機體便失去了維持血糖穩(wěn)定的核心調(diào)控機制,患者只能依賴外源性胰島素來維持生命。
然而,傳統(tǒng)的胰島素替代療法雖然能夠延續(xù)患者的生命,卻難以模擬人體自然的精細化血糖調(diào)控。長期依賴注射往往伴隨血糖大幅波動,增加了低血糖和高血糖的風險,也為心血管、腎臟和神經(jīng)等慢性并發(fā)癥埋下隱患。
要真正理解干細胞如何參與修復(fù),就必須抓住兩個核心問題:一是免疫系統(tǒng)為何會發(fā)動這場“錯誤的戰(zhàn)爭”;二是β細胞喪失后,機體在血糖調(diào)控上遭受了怎樣的破壞。也正因此,如何在重建β細胞功能的同時抑制免疫攻擊,成為破解1型糖尿病的關(guān)鍵突破口。
干細胞治療1型糖尿病的三大核心機制
干細胞主要是通過以下三大類機制協(xié)同作用,實現(xiàn)對1型糖尿病的根本性修復(fù):
- 免疫調(diào)節(jié):調(diào)控紊亂的免疫系統(tǒng),抑制對β細胞的自身免疫攻擊,從根源上阻止疾病進展。
- 細胞替代:通過定向分化功能性胰島β細胞,直接替代被破壞的細胞,重建內(nèi)源性胰島素分泌系統(tǒng)。
- 微環(huán)境與旁分泌:通過分泌多種生物活性因子,改善胰島局部微環(huán)境,促進血管新生和組織修復(fù),為細胞存活和功能恢復(fù)提供支持。
深入解析三大核心機制的作用形式
機制一:干細胞的免疫調(diào)節(jié)機制,阻斷自身免疫攻擊
干細胞能夠通過??直接接觸??、??分泌可溶性因子??(如TGF-β、IL-10)及??外泌體(EVs)?? 三種方式調(diào)控免疫微環(huán)境,抑制自身免疫攻擊,保護胰島β細胞。其核心機制包括:
1.??調(diào)節(jié)T細胞平衡??:干細胞在改善免疫失衡方面最突出的作用就是對T細胞的調(diào)控。它們能抑制效應(yīng)T細胞(Teff)的過度增殖和殺傷力,減少對β細胞的直接攻擊;與此同時,又能促進調(diào)節(jié)性T細胞(Tregs)的擴增,幫助免疫系統(tǒng)重新建立“耐受”。
研究顯示,接受干細胞治療后,Treg比例可顯著提升,而這種作用主要依賴于TGF-β和IL-10等信號通路。
2.??調(diào)控B細胞功能??:除了T細胞,B細胞也是1型糖尿病發(fā)生中的重要推手。干細胞能夠在炎癥環(huán)境下抑制B細胞的過度活化,減少自身抗體(如IgG、IgM)的產(chǎn)生,從而減輕其對β細胞的持續(xù)損傷。
但在穩(wěn)態(tài)情況下,它們并不會完全“關(guān)閉”B細胞功能,而是維持其正常免疫作用,這種差異化調(diào)控與干細胞來源和所處微環(huán)境密切相關(guān)。
3.??重塑巨噬細胞表型??:干細胞還能影響巨噬細胞的性格,使其由促炎的M1型逐漸轉(zhuǎn)向具有修復(fù)作用的M2型,從而緩解胰島局部炎癥。
外泌體在這一過程中起到關(guān)鍵作用,其中攜帶的miR-21-5p等分子能夠抑制NF-κB信號通路,降低TNF-α、IL-6等促炎因子的水平,為β細胞提供一個更有利的生存環(huán)境。
4.??抑制樹突狀細胞(DC)成熟??:樹突狀細胞作為抗原呈遞的關(guān)鍵角色,在T細胞異常激活中扮演了推手。干細胞能下調(diào)CD80、CD86等共刺激分子的表達,削弱樹突狀細胞的成熟度和激活能力。
同時,它們還能阻止樹突狀細胞遷移至淋巴器官,從源頭上減少新的T細胞被激活,從而降低對β細胞的進一步攻擊。
機制二:關(guān)鍵信號通路與微環(huán)境改善?
干細胞和它們釋放的外泌體并不是憑空“安撫”免疫系統(tǒng),而是通過一整套分子通路來重塑胰島的小環(huán)境——讓炎癥降溫、讓保護性的細胞上崗、讓移植或再生的β細胞有活下去的機會。下面幾條信號通路是常被提到的關(guān)鍵節(jié)點,它們互相配合,共同創(chuàng)造一個有利于β細胞存活與功能恢復(fù)的微環(huán)境。
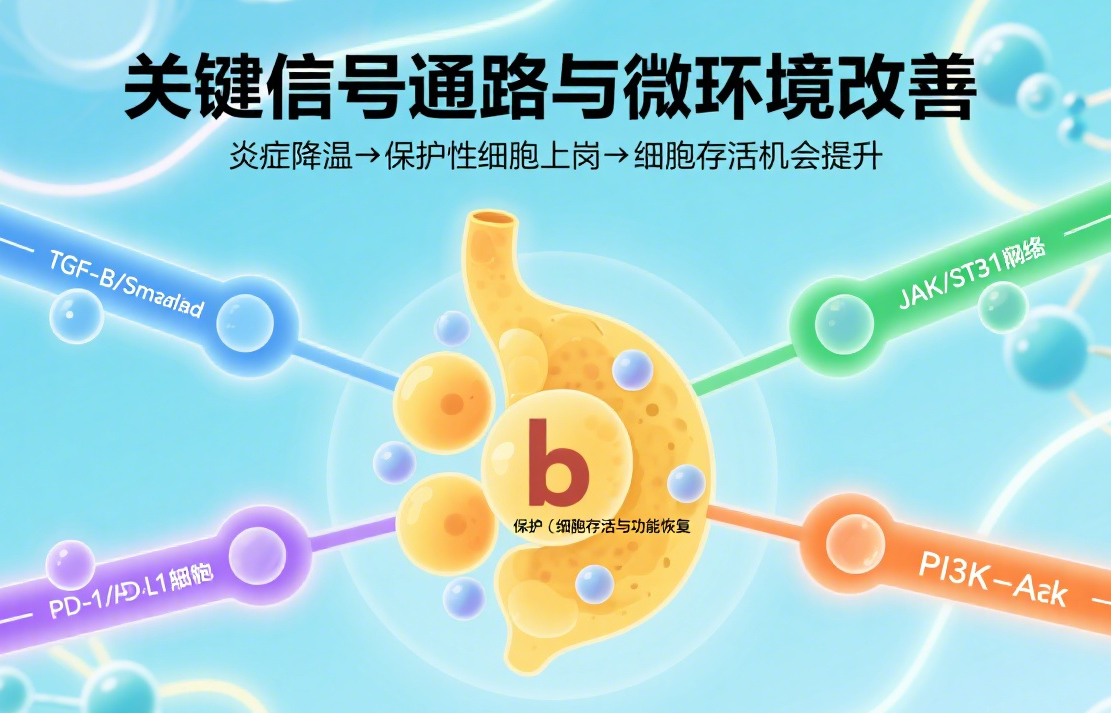
TGF-β/Smad通路:干細胞會分泌TGF-β,激活細胞內(nèi)的Smad蛋白家族,從而推動調(diào)節(jié)性T細胞(Tregs)生成并促使巨噬細胞向修復(fù)型(M2)轉(zhuǎn)化;簡單說,就是既抑制炎癥的“火勢”,又增加修復(fù)的“力量”,從而減輕胰島周圍的免疫壓力。
JAK/STAT3通路:像IL-10這樣的抗炎因子通過 JAK/STAT3 路徑發(fā)揮作用,能快速下調(diào)促炎分子的表達并推動巨噬細胞走向抗炎表型。這條通路在把免疫反應(yīng)從“攻擊模式”拉回“修復(fù)模式”上,起到很直接的分子橋梁作用。
PD-1/PD-L1軸:干細胞或其衍生物可以上調(diào)PD-L1表達,與T細胞表面的PD-1結(jié)合后抑制TCR的過度激活——換句話說,這是一種“給T細胞按下剎車”的機制,能有效減少對β細胞的持續(xù)攻擊。
PI3K/Akt路徑與細胞生存信號:PI3K/Akt 路徑更多地參與細胞存活、抗凋亡和代謝調(diào)節(jié)。干細胞通過激活這一路徑幫助胰島細胞抵抗壓力刺激、降低凋亡傾向,從而提高移植或再生細胞的成活率和功能穩(wěn)定性。
總體來看,這些通路不是孤立起作用,而是交織成網(wǎng):免疫抑制、促修復(fù)和增強細胞存活三條線同時發(fā)力,最終把胰島的小環(huán)境從“敵對”逐步改造成“可居住”的狀態(tài)。
機制三:促進β細胞再生的雙重策略
干細胞療法促進β細胞再生主要通過兩條互補的路線協(xié)同發(fā)揮作用。
一條是細胞替代:用人多能干細胞(hPSC,包括 iPSC 與 ESC)分化出能響應(yīng)葡萄糖的胰島β細胞或其前體,移植回體內(nèi)以恢復(fù)胰島素分泌。現(xiàn)在更常見的做法是把細胞分化到胰腺祖細胞(PP)階段再移植,讓體內(nèi)信號來完成最后的成熟;這種方法便于規(guī)模化生產(chǎn),但難點在于如何確保移植后細胞能穩(wěn)定成熟、存活并長期開機運轉(zhuǎn)。
另一條是免疫調(diào)節(jié)+激活內(nèi)源再生:以間充質(zhì)干細胞(MSC)等為代表,通過抑制局部炎癥、分泌生長因子和外泌體,既保護殘存的β細胞不被繼續(xù)攻擊,又能誘導(dǎo)胰腺內(nèi)在祖細胞或殘余β細胞再生。
把兩條路線結(jié)合起來(比如共移植、封裝并提供免疫保護)是目前被廣泛看好的策略:既“補細胞”,也“護細胞”,更有望實現(xiàn)長期穩(wěn)態(tài)的恢復(fù)。
對未來1型糖尿病技術(shù)路線的啟示
深入理解干細胞修復(fù)胰島的機制,會直接指引下一代技術(shù)的研發(fā)方向,下面三條比較具有可操作性的思路值得關(guān)注:
代謝成熟訓練 — 用“生理節(jié)律”把細胞訓練成真細胞:基于對β細胞代謝耦合與電生理激活的理解,研究者可以在分化后期引入模擬生理的葡萄糖脈沖或代謝應(yīng)激訓練,讓細胞在“上下班”的節(jié)律中逐步建立起成熟的能量代謝和鈣流響應(yīng),這比一次性化學促分化更接近天然成熟路徑,可能顯著提高移植后功能穩(wěn)定性。
智能基質(zhì)與可控釋放 — 同時給細胞“房子”和“營養(yǎng)”:根據(jù)細胞外基質(zhì)(ECM)和旁分泌信號對細胞命運的影響,可開發(fā)仿生水凝膠或智能支架,不僅提供三維支撐,還能按需釋放生長因子、促血管化因子或免疫調(diào)節(jié)分子。這樣的基質(zhì)既有利于細胞黏附、分化與血管接入,也能在早期移植窗口期主動抑制局部炎癥。
基因工程化的免疫“隱形”策略 — 從源頭降低排斥風險:針對自身免疫與移植排斥兩重挑戰(zhàn),可以用基因編輯在供體細胞上做“減法與加法”:敲低或敲除特定HLA表達以降低抗原性,同時過表達PD-L1、CD47或HLA-G等免疫調(diào)節(jié)分子以抑制T細胞和吞噬細胞反應(yīng)。這樣的“通用型”或“免疫隱形”胰島細胞,配合局部免疫調(diào)節(jié)技術(shù),能顯著降低長期免疫抑制的需求。
結(jié)語
干細胞修復(fù)1型糖尿病是一個多機制、多步驟協(xié)同作用的復(fù)雜過程。核心在于功能性β細胞的定向分化與成熟、免疫耐受的成功誘導(dǎo)以及支持性微環(huán)境的有效構(gòu)建三者缺一不可。
對作用機制的深刻理解,是推動該領(lǐng)域從基礎(chǔ)研究走向臨床應(yīng)用的基石。當前研究表明,結(jié)合基因編輯技術(shù)的“免疫豁免型”通用型細胞療法以及基于外泌體的無細胞治療策略,可能是未來極具潛力的研究方向。
參考資料:
[1]Farooq, T., Rehman, K., Hameed, A., Akash, M.S.H. (2018). Stem Cell Therapy and Type 1 Diabetes Mellitus: Treatment Strategies and Future Perspectives. In: Pham, P. (eds) Tissue Engineering and Regenerative Medicine. Advances in Experimental Medicine and Biology(), vol 1084. Springer, Cham. https://doi.org/10.1007/5584_2018_195
[2]Hunault, L., Hesselson, D. Finishing the odyssey to a stem cell cure for type 1 diabetes.?npj Metab Health Dis?2, 9 (2024). https://doi.org/10.1038/s44324-024-00014-5
[3]Wang, C., Wu, Y. & Jiang, J. The role and mechanism of mesenchymal stem cells in immunomodulation of type 1 diabetes mellitus and its complications: recent research progress and challenges: a review.?Stem Cell Res Ther?16, 308 (2025). https://doi.org/10.1186/s13287-025-04431-1
免責說明:本文僅用于傳播科普知識,分享行業(yè)觀點,不構(gòu)成任何臨床診斷建議!杭吉干細胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請隨時聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信