肌萎縮側(cè)索硬化癥(ALS)是一種累及上、下運(yùn)動神經(jīng)元的進(jìn)行性神經(jīng)退行性疾病,嚴(yán)重影響患者的生活質(zhì)量。該疾病涉及遺傳與環(huán)境因素之間復(fù)雜的相互作用,這給治療研發(fā)帶來了巨大挑戰(zhàn)。目前可用于ALS的疾病修飾藥物療效有限,僅能輕微延緩疾病進(jìn)展。

肌萎縮側(cè)索硬化癥的多元治療方法——藥物、基因與干細(xì)胞療法的進(jìn)展與展望
近期,已獲批藥物AMX0035的撤市,進(jìn)一步凸顯了該領(lǐng)域面臨的困境。與此同時,針對ALS及相關(guān)神經(jīng)退行性疾病的生物靶點(diǎn)研究,為治療干預(yù)提供了獨(dú)特切入點(diǎn)。隨著基因工程等技術(shù)的進(jìn)步,干細(xì)胞療法和基因療法等創(chuàng)新療法也備受關(guān)注,為ALS的治療帶來了新的希望。
此外,對ALS癥狀的有效管理,對于改善患者的日常生活至關(guān)重要。近日,期刊《Frontiers in Neurology》發(fā)表了一篇題為“肌萎縮側(cè)索硬化癥的當(dāng)前和新興治療策略:從藥物治療到基因和干細(xì)胞療法”的研究綜述,旨在對這一快速發(fā)展領(lǐng)域進(jìn)行重點(diǎn)梳理[1]。
該綜述總結(jié)了已獲批及新興藥物治療的機(jī)制、療效與局限性;分析了干細(xì)胞與基因治療的原理、當(dāng)前進(jìn)展與挑戰(zhàn),并特別強(qiáng)調(diào)了針對散發(fā)性ALS進(jìn)行治療的必要性;最后,文章也突出了綜合癥狀管理在患者照護(hù)中不可或缺的作用。
藥物治療肌萎縮側(cè)索硬化癥的進(jìn)展
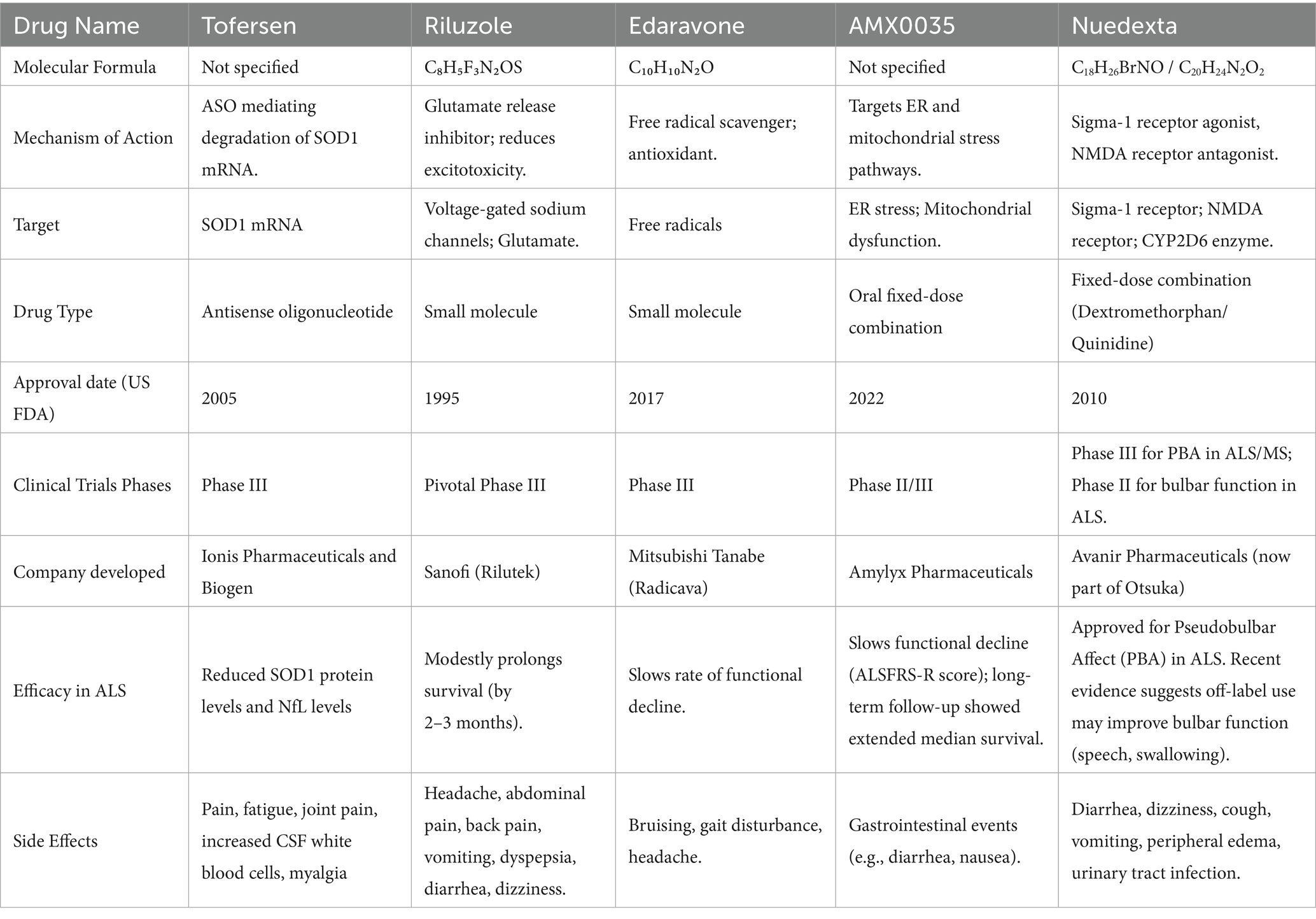
肌萎縮側(cè)索硬化癥(ALS)藥物治療領(lǐng)域的進(jìn)展已催生出一些疾病修飾療法。目前,包括利魯唑、依達(dá)拉奉和AMX0035在內(nèi)的三種藥物已獲得FDA批準(zhǔn)(表1)。值得注意的是,AMX0035的III期PHOENIX試驗結(jié)果并不理想,生產(chǎn)商已啟動市場撤回程序。此外,Tofersen已獲得加速批準(zhǔn),但仍需在正在進(jìn)行的試驗中進(jìn)一步證實其臨床療效。鑒于現(xiàn)有指南尚未納入Tofersen等最新獲批藥物,因此,根據(jù)患者個體情況定制治療方案至關(guān)重要。
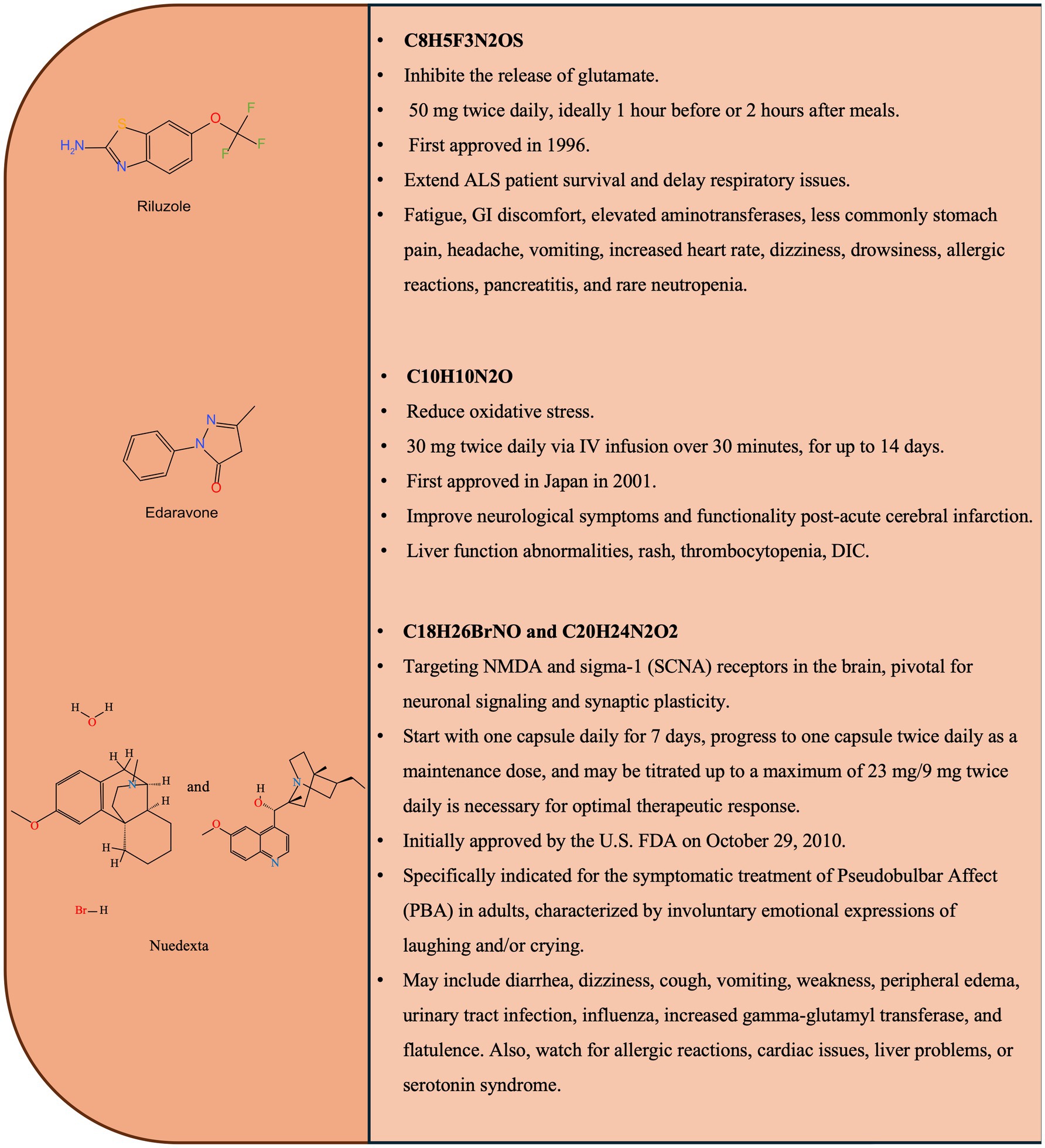
利魯唑:經(jīng)典藥物,通過調(diào)節(jié)谷氨酸與抑制興奮性毒性實現(xiàn)有限的生存獲益
利魯唑是首個獲批的ALS基礎(chǔ)治療藥物,利魯唑的化學(xué)結(jié)構(gòu)和主要特征如圖1所示。其核心作用機(jī)制在于調(diào)節(jié)谷氨酸穩(wěn)態(tài)以對抗興奮性毒性。它通過阻斷電壓門控鈉通道減少谷氨酸釋放,并促進(jìn)其攝取,從而降低細(xì)胞外谷氨酸水平,保護(hù)神經(jīng)元。
此外,它也對鈣穩(wěn)態(tài)、氧化應(yīng)激和細(xì)胞凋亡途徑有調(diào)節(jié)作用。臨床試驗證實,該藥可延長患者中位生存期約2至3個月,并延緩呼吸功能衰退,但其臨床獲益有限。真實世界療效證據(jù)存在爭議,且使用時需密切監(jiān)測肝功能等潛在不良反應(yīng)。
依達(dá)拉奉:以抗氧化應(yīng)激為核心機(jī)制,其療效證據(jù)存在顯著的地域性差異
依達(dá)拉奉是一種自由基清除劑,其治療ALS的主要機(jī)制是通過強(qiáng)大的抗氧化活性,抑制脂質(zhì)過氧化并清除羥自由基等有害活性氧,從而減輕氧化應(yīng)激導(dǎo)致的神經(jīng)元損傷。它在日本和美國獲批用于治療,尤其是早期ALS患者。
然而,其療效證據(jù)并不一致:關(guān)鍵臨床試驗顯示其能延緩功能下降,但部分真實世界研究(特別是來自印度的報告)未能證實其對功能評分或生存率的顯著改善。這種差異可能與患者群體異質(zhì)性有關(guān),其全球適用性仍需進(jìn)一步評估。
AMX0035:靶向雙通路的聯(lián)合療法,其早期積極療效信號未能在關(guān)鍵III期試驗中得到證實
AMX0035是由苯丁酸鈉和牛磺熊去氧膽酸組成的復(fù)方制劑,旨在通過同時緩解內(nèi)質(zhì)網(wǎng)應(yīng)激和線粒體功能障礙這一雙通路策略來保護(hù)神經(jīng)元。基于顯示其能延緩疾病進(jìn)展和延長生存期的II期試驗結(jié)果,它曾獲得有條件批準(zhǔn)。
然而,隨后的確證性III期臨床試驗未能達(dá)到延緩功能衰退的主要療效終點(diǎn),這凸顯了在更廣泛患者群體中復(fù)制早期積極結(jié)果的挑戰(zhàn)。該藥物最終因此自愿撤市,但其研發(fā)歷程為ALS藥物開發(fā)提供了重要經(jīng)驗。
Tofersen:針對SOD1突變的精準(zhǔn)基因療法,開創(chuàng)了基于生物標(biāo)志物改善的加速批準(zhǔn)范式
Tofersen是一種反義寡核苷酸藥物,專門用于治療攜帶SOD1基因突變的ALS患者。其作用機(jī)制是精準(zhǔn)靶向并與SOD1mRNA結(jié)合,導(dǎo)致其降解,從而從源頭上減少有毒SOD1蛋白的生成。
盡管關(guān)鍵III期臨床試驗在主要臨床功能終點(diǎn)上未顯示顯著差異,但該藥能顯著降低腦脊液SOD1蛋白和血漿神經(jīng)絲輕鏈(神經(jīng)元損傷的關(guān)鍵生物標(biāo)志物)水平。基于這一確切的生物標(biāo)志物效應(yīng),Tofersen于2023年獲得FDA加速批準(zhǔn),成為ALS精準(zhǔn)治療和基于生物標(biāo)志物審批的重要里程碑。
Nuedexta:主要用于治療假性延髓麻痹的復(fù)方制劑,其潛在的神經(jīng)保護(hù)作用仍在探索中
Nuedexta是右美沙芬和奎尼丁的復(fù)方制劑,已獲批用于治療ALS等疾病相關(guān)的假性延髓麻痹(PBA),即無法控制的大笑或哭泣。其作用機(jī)制是通過右美沙芬調(diào)節(jié)與情緒相關(guān)的神經(jīng)遞質(zhì)傳遞(奎尼丁則用于提高右美沙芬的生物利用度),從而穩(wěn)定情緒反應(yīng)。
此外,右美沙芬對σ-1受體及谷氨酸興奮性毒性的潛在作用,使其可能具備一定的神經(jīng)保護(hù)功能,并可能對延髓功能(如言語、吞咽)有支持作用,但這方面的治療前景仍在研究之中。
二、肌萎縮側(cè)索硬化癥潛在的治療靶點(diǎn)
研究人員正在深入探索一系列生物靶點(diǎn),以對抗肌萎縮側(cè)索硬化癥(ALS)及相關(guān)神經(jīng)退行性疾病,每個靶點(diǎn)都為治療干預(yù)提供了獨(dú)特的途徑。潛在治療肌萎縮側(cè)索硬化癥(ALS,俗稱“漸凍癥”)的靶點(diǎn)主要圍繞疾病的核心病理機(jī)制展開,可分為以下幾類:
- 興奮性毒性調(diào)控靶點(diǎn):靶向離子通道(如鈉、鉀、鈣通道)和谷氨酸受體,旨在抑制谷氨酸的過度釋放或作用,從而減輕其對神經(jīng)元的興奮性毒性損傷。
- 神經(jīng)炎癥調(diào)控靶點(diǎn):針對中樞神經(jīng)系統(tǒng)內(nèi)過度激活的免疫反應(yīng),重點(diǎn)是小膠質(zhì)細(xì)胞的異常活化及相關(guān)促炎因子,以減輕炎癥對神經(jīng)元的損害。
- 氧化應(yīng)激平衡靶點(diǎn):旨在增強(qiáng)內(nèi)源性抗氧化防御系統(tǒng),例如提升超氧化物歧化酶(SOD)、谷胱甘肽過氧化物酶(GPx)等酶的活性,以對抗過量的活性氧造成的神經(jīng)元損傷。
- 蛋白質(zhì)穩(wěn)態(tài)與清除靶點(diǎn):針對錯誤折疊蛋白(如TDP-43)在細(xì)胞質(zhì)中的異常聚集,策略包括激活自噬-溶酶體通路以清除聚集體,或利用分子伴侶等質(zhì)量控制因子促進(jìn)蛋白質(zhì)正確折疊。
- 神經(jīng)營養(yǎng)因子支持靶點(diǎn):通過基因治療或藥物手段,提高腦源性神經(jīng)營養(yǎng)因子(BDNF)、膠質(zhì)細(xì)胞系衍生神經(jīng)營養(yǎng)因子(GDNF)等因子的水平,以增強(qiáng)神經(jīng)元的存活能力和功能。
- 線粒體功能與代謝靶點(diǎn):聚焦于改善線粒體功能失調(diào)和能量代謝異常,通過恢復(fù)能量供應(yīng)和細(xì)胞代謝穩(wěn)態(tài)來支持神經(jīng)元生存。
- 廣泛病理過程的共性靶點(diǎn):特別強(qiáng)調(diào)針對在超過95% ALS病例(包括散發(fā)性ALS)中出現(xiàn)的共同病理特征,其中TDP-43蛋白病是關(guān)鍵核心靶點(diǎn)。此外,持續(xù)的神經(jīng)炎癥、氧化應(yīng)激和線粒體功能障礙也被視為適用于廣大患者群體的重要干預(yù)節(jié)點(diǎn)。
綜上所述,當(dāng)前的潛在治療靶點(diǎn)不僅包括針對特定致病蛋白(如SOD1、TDP-43)的精準(zhǔn)干預(yù),更著重于開發(fā)能廣泛調(diào)節(jié)上述共有病理過程的療法,這對治療占多數(shù)的散發(fā)性ALS患者尤為重要。
三、治療肌萎縮側(cè)索硬化癥的創(chuàng)新療法
01、干細(xì)胞療法治療肌萎縮側(cè)索硬化癥
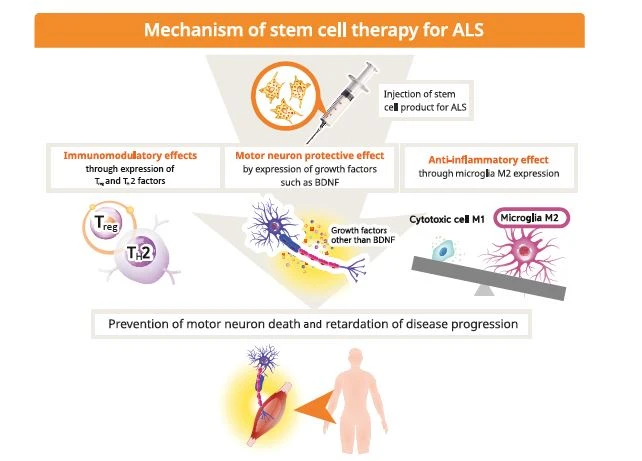
干細(xì)胞療法是治療肌萎縮側(cè)索硬化癥(ALS)的新興前沿領(lǐng)域,旨在提供神經(jīng)保護(hù)、調(diào)節(jié)神經(jīng)炎癥并有可能修復(fù)受損的運(yùn)動神經(jīng)元(圖2)。該策略利用多種細(xì)胞類型,包括間充質(zhì)干細(xì)胞(MSCs)、神經(jīng)干細(xì)胞(NSCs)和誘導(dǎo)多能干細(xì)胞(iPSCs)。
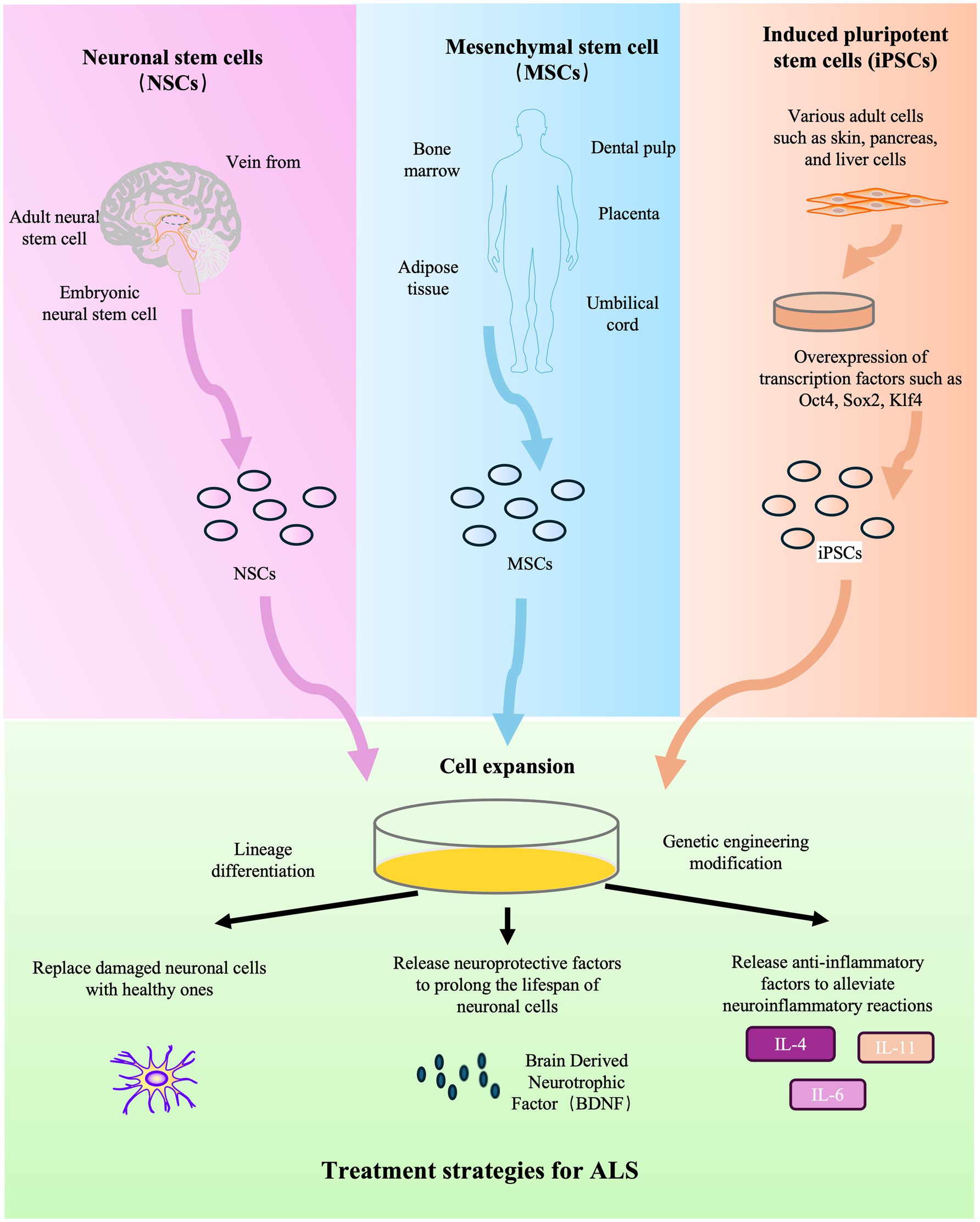
臨床前基礎(chǔ)和機(jī)制:動物模型研究已為該療法奠定了理論基礎(chǔ)。利用SOD1G93A轉(zhuǎn)基因小鼠等模型的研究表明,干細(xì)胞移植可以減輕神經(jīng)炎癥并提供營養(yǎng)支持。例如,在這些模型中,間充質(zhì)干細(xì)胞移植已被證明可以通過抑制有害免疫細(xì)胞的活化來調(diào)節(jié)神經(jīng)炎癥環(huán)境。
此外,干細(xì)胞為遞送神經(jīng)營養(yǎng)因子提供了一個平臺。例如,經(jīng)基因工程改造、可分泌膠質(zhì)細(xì)胞系衍生神經(jīng)營養(yǎng)因子(GDNF)的神經(jīng)祖細(xì)胞已在臨床前研究中得到探索。這些研究表明,益處可能不僅來自潛在的細(xì)胞替代,還源于強(qiáng)大的旁分泌效應(yīng)。
然而,移植細(xì)胞在ALS微環(huán)境中長期存活和整合等挑戰(zhàn),仍是臨床前模型面臨的重大障礙。生物材料與干細(xì)胞的結(jié)合也作為一種新方法在臨床前研究中被探索。除了直接治療,干細(xì)胞還被用于體外模擬ALS,從而深入揭示疾病機(jī)制并發(fā)現(xiàn)新的治療靶點(diǎn)。
干細(xì)胞治療漸凍癥的臨床轉(zhuǎn)化:試驗與挑戰(zhàn):轉(zhuǎn)化到人體試驗已經(jīng)歷了多個階段,早期研究主要評估安全性和可行性。
2021年,《肌肉與神經(jīng)主頁》發(fā)表了一項“隨機(jī)、安慰劑對照的3期臨床研究,旨在評估間充質(zhì)干細(xì)胞誘導(dǎo)分泌高水平神經(jīng)營養(yǎng)因子治療肌萎縮側(cè)索硬化癥的效果[2]。

總體而言,MSC-NTF治療耐受性良好,未出現(xiàn)安全性問題。28周時,MSC-NTF組和安慰劑組分別有33%和28%的受試者達(dá)到臨床應(yīng)答標(biāo)準(zhǔn),因此未達(dá)到主要終點(diǎn)。對基線ALSFRS-R評分≥35的受試者(n=58)進(jìn)行的預(yù)設(shè)分析顯示,28周時MSC-NTF組的臨床應(yīng)答率為35%,安慰劑組為16%。MSC-NTF組在腦脊液中神經(jīng)炎癥、神經(jīng)退行性變和神經(jīng)營養(yǎng)因子支持相關(guān)的生物標(biāo)志物方面觀察到顯著改善,而安慰劑組未見變化。
2022年,一項將分泌GDNF的人類神經(jīng)祖細(xì)胞移植到ALS患者脊髓中:一項1/2a期試驗表明,將分泌GDNF的人類神經(jīng)祖細(xì)胞(CNS10-NPC-GDNF)移植到脊髓中,在42個月內(nèi)是可行且安全的,并且未對運(yùn)動功能產(chǎn)生負(fù)面影響[3]。

2025年9月18日,韓國CorestemChemon Inc.公司宣布它已在澳大利亞墨爾本舉行的PACTALS 2025大會上展示了Neuronata-R ? (lenzumestrocel) 第三階段ALSummit試驗的完整結(jié)果,用于治療漸凍癥 (ALS) [4]。
雖然整體試驗未能達(dá)到設(shè)定的主要和次要終點(diǎn),但結(jié)果顯示:在疾病進(jìn)展較慢的ALS患者中,Neuronata-R?展現(xiàn)出了顯著的療效。
并且該公司將在2026年前向美國食品藥品監(jiān)督管理局(FDA)提交生物制品許可申請,縮短傳統(tǒng)臨床試驗周期,更快惠及患者。
這些臨床試驗正在認(rèn)真評估各種干細(xì)胞類型和移植策略的安全性、可行性和有效性。臨床轉(zhuǎn)化面臨的常見挑戰(zhàn)包括免疫排斥、患者反應(yīng)的個體差異以及對標(biāo)準(zhǔn)化細(xì)胞產(chǎn)品和遞送方案的需求。其對疾病進(jìn)程和生存率的決定性影響仍有待研究,這凸顯了開展更多設(shè)計嚴(yán)謹(jǐn)?shù)呐R床研究的必要性。
02、肌萎縮側(cè)索硬化癥的基因治療
基因治療已成為ALS領(lǐng)域極具前景的方向,主要策略包括基因沉默、基因編輯及神經(jīng)營養(yǎng)因子遞送(圖3)。
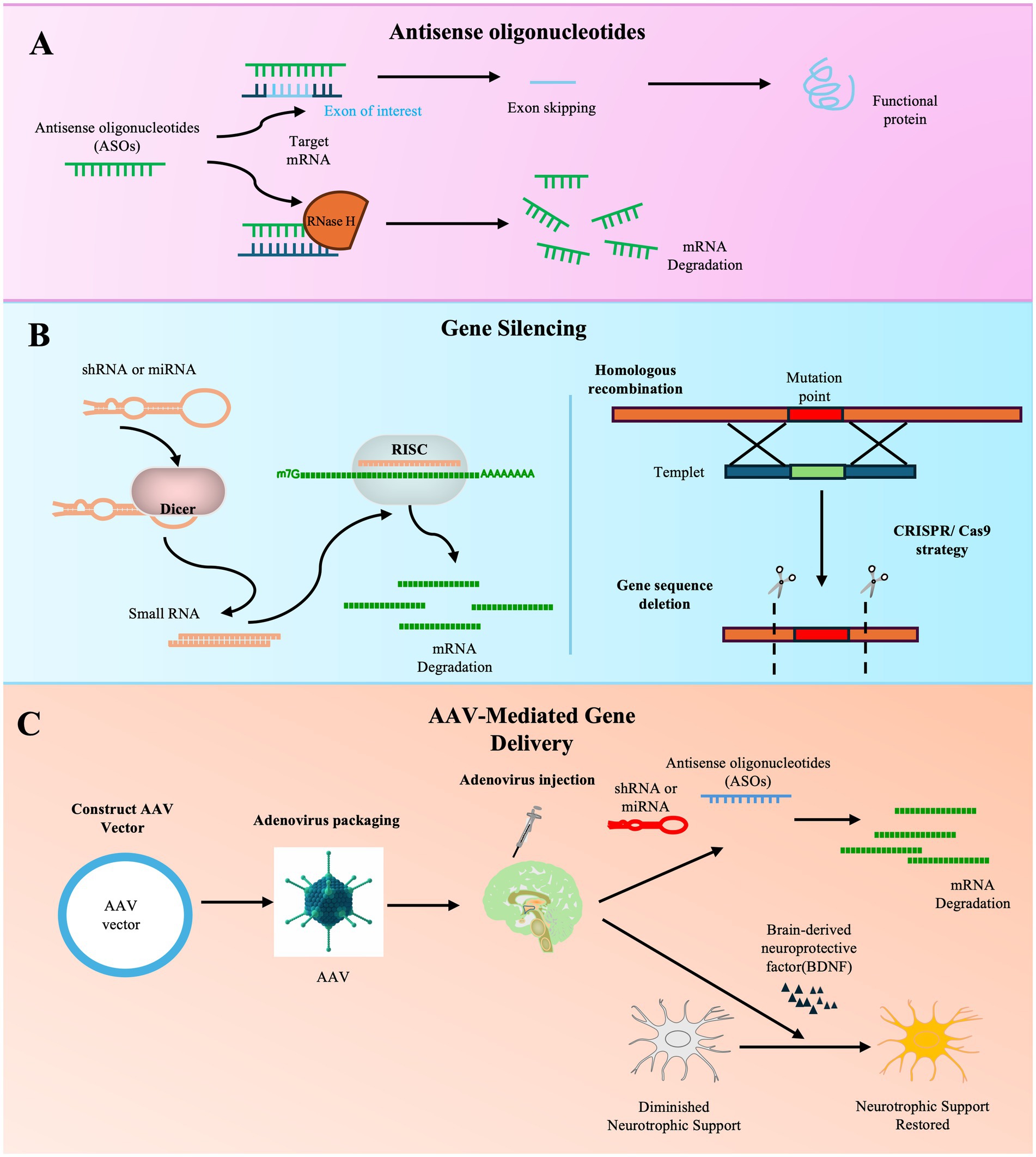
反義寡核苷酸療法的進(jìn)展:針對SOD1的托弗森是ASO療法的代表,其基于生物標(biāo)志物改善獲加速批準(zhǔn),標(biāo)志著重要突破。目前,針對C9orf72、FUS、ATXN2等其他基因靶點(diǎn)的ASO候選藥物也正處于多項臨床試驗階段,顯示出該策略在遺傳型ALS中的持續(xù)拓展。
AAV載體遞送與其他策略:腺相關(guān)病毒載體介導(dǎo)的基因遞送在臨床前研究中取得進(jìn)展。例如,通過脊髓軟膜下注射AAV9可實現(xiàn)廣泛的中樞神經(jīng)系統(tǒng)基因沉默,在ALS動物模型中有效延緩運(yùn)動神經(jīng)元退化。同時,針對散發(fā)性ALS常見下游病理(如TDP-43蛋白異常)的基因調(diào)控策略正在探索,例如校正TDP-43依賴性STMN2剪接異常的ASO在臨床前模型中展現(xiàn)出潛力。此外,AAV遞送神經(jīng)營養(yǎng)因子等支持性療法也為運(yùn)動神經(jīng)元存活提供了新思路。
挑戰(zhàn)與未來方向:基因治療仍面臨多重挑戰(zhàn),包括遞送系統(tǒng)對中樞神經(jīng)系統(tǒng)的覆蓋效率、基因編輯的精準(zhǔn)度與脫靶風(fēng)險控制。根本性難題在于,約占病例90%的散發(fā)性ALS缺乏明確單基因靶點(diǎn),使得患者分層困難,療法開發(fā)需兼顧多病理通路。未來可能需要通過多靶點(diǎn)協(xié)同治療策略,并結(jié)合個體化醫(yī)療手段,方有望將ALS轉(zhuǎn)變?yōu)榭煽氐穆约膊 ?/p>
四、肌萎縮側(cè)索硬化癥的癥狀管理
ALS的癥狀管理對于直接提升患者生活質(zhì)量和心理福祉具有核心價值。疾病不僅導(dǎo)致運(yùn)動功能喪失,還常伴隨情緒波動、抑郁焦慮、肌肉抽搐、疼痛、疲勞、睡眠障礙、流涎及便秘等廣泛的身心癥狀。盡管許多對癥藥物缺乏強(qiáng)效證據(jù),但積極管理能顯著緩解患者痛苦,是全程照護(hù)中與疾病修飾療法同等重要的支柱。
管理的關(guān)鍵尤其體現(xiàn)在對呼吸衰竭和營養(yǎng)衰竭這兩個核心問題的干預(yù)上。臨床試驗證實,無創(chuàng)通氣不僅能平均延長生存期,更是改善生活質(zhì)量的關(guān)鍵。同時,針對吞咽困難(及時啟動腸內(nèi)營養(yǎng))及肌肉痙攣(常用藥物如巴氯芬)的有效管理,直接關(guān)系到患者的生存安全與身體機(jī)能。這些個體化的支持性治療旨在動態(tài)響應(yīng)患者需求,根本目標(biāo)是在疾病各階段最大化其生活質(zhì)量,并為照護(hù)者提供支持,實現(xiàn)富有同理心的整體護(hù)理。
五、討論與結(jié)論
眾多綜述已概述了ALS的病理生理與治療進(jìn)展。本綜述的獨(dú)特價值在于,及時且批判性地分析了該領(lǐng)域近年的范式轉(zhuǎn)變(結(jié)合2023-2025年發(fā)展)。
這一轉(zhuǎn)變體現(xiàn)為“雙重戰(zhàn)略”框架的構(gòu)建:一方面,是以Tofersen為代表的、基于生物標(biāo)志物的精準(zhǔn)基因沉默療法,為特定遺傳亞型帶來突破;另一方面,是針對缺乏明確基因靶點(diǎn)的絕大多數(shù)散發(fā)性患者,轉(zhuǎn)向開發(fā)調(diào)節(jié)TDP-43蛋白病、神經(jīng)炎癥等共通下游病理的廣譜機(jī)制療法。
干細(xì)胞療法則被定位為該框架中的重要探索方向,認(rèn)可其在臨床前研究中展現(xiàn)的神經(jīng)保護(hù)與免疫調(diào)節(jié)潛力,但也指出了其面臨的細(xì)胞存活、整合及長期安全性等挑戰(zhàn)。
通過對Tofersen的加速批準(zhǔn)、AMX0035的III期失敗以及細(xì)胞療法的前景與難題進(jìn)行并置分析,本文清晰地勾勒出當(dāng)前療法從研發(fā)到臨床轉(zhuǎn)化的復(fù)雜全景。討論尖銳地指出,Tofersen的成功反而凸顯了約90%散發(fā)性ALS患者的“靶點(diǎn)困境”。
因此,未來的“精準(zhǔn)性”必須超越單一基因靶向,邁向基于生物標(biāo)志物的病理分型。在此背景下,基于機(jī)制的藥物與干細(xì)胞療法扮演互補(bǔ)角色:前者精確調(diào)控特定異常通路,后者則可能提供廣泛的支持性微環(huán)境。兩者的成功應(yīng)用都極度依賴于生物標(biāo)志物的進(jìn)步,以實現(xiàn)對高度異質(zhì)患者群體的有效分層。
最終,本文構(gòu)建了一個基因療法、細(xì)胞療法、藥物療法與支持護(hù)理深度融合的未來協(xié)同框架:
- 精準(zhǔn)打擊:對明確遺傳亞型使用基因沉默或編輯療法。
- 環(huán)境重塑與系統(tǒng)支持:對散發(fā)型患者,探索將調(diào)節(jié)特定通路的靶向藥物與具有廣譜支持作用的細(xì)胞療法相結(jié)合。
- 全程基石:所有疾病修飾療法都必須與全方位的支持性護(hù)理深度整合,以直接改善生活質(zhì)量和生存結(jié)局。
盡管挑戰(zhàn)巨大,但通過生物標(biāo)志物指導(dǎo)的患者分層,并靈活組合基因工具、細(xì)胞載體、藥物分子及支持護(hù)理,這一綜合策略旨在將ALS逐步轉(zhuǎn)變?yōu)橐环N可管理的慢性疾病。細(xì)胞療法在其中扮演著不可替代的“環(huán)境調(diào)節(jié)者”和“系統(tǒng)支持者”角色,是填補(bǔ)當(dāng)前治療空白的關(guān)鍵探索方向。
參考資料:
[1]:Wang Z, Huang J and Yun D (2026) Current and emerging therapeutic strategies for amyotrophic lateral sclerosis: from pharmacological approaches to gene and stem cell therapies. Front. Neurol. 17:1729302. doi: 10.3389/fneur.2026.1729302
[2]:https://onlinelibrary.wiley.com/doi/10.1002/mus.27472
[3]:https://www.nature.com/articles/s41591-022-01956-3
[4]:https://www.nature.com/articles/d43747-020-00727-8
免責(zé)說明:本文僅用于傳播科普知識,分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請隨時聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信