描述:2026年《帕金森病雜志》綜述揭示:從胎兒腹側中腦多巴胺能神經元移植,到PSC(胚胎/誘導多能干細胞)衍生vmDA祖細胞臨床試驗,細胞療法歷經數十年演進。早期試驗曾出現移植誘發性運動障礙(GID)及α-突觸核蛋白病理蔓延,但后續研究明確了理想患者特征。當前全球多項I/II期試驗顯示短期安全性良好,但細胞存活率低(約5%)、1?F-DOPA攝取未恢復正常。III期試驗已啟動,仍需優化劑量、遞送及免疫抑制方案。
一、帕金森病與細胞療法的邏輯
帕金森病(PD)是一種常見的神經退行性疾病。其病理特征有二:一是路易小體與路易神經突中α-突觸核蛋白的異常積聚;二是黑質腹側中腦多巴胺能(vmDA)神經元的進行性凋亡。后者負責調控運動機能,其喪失直接導致了震顫、僵硬與動作遲緩等典型運動障礙。
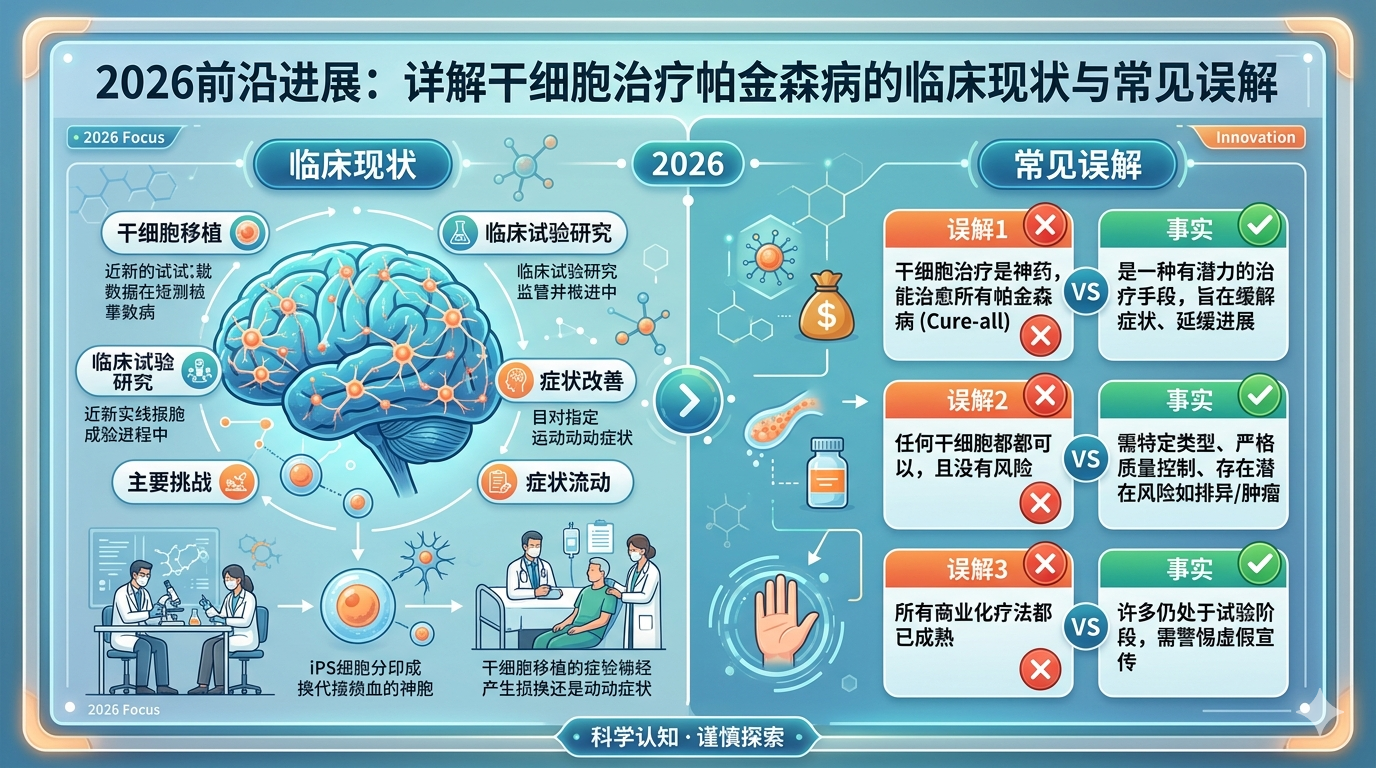
病程早期,上述癥狀通常可被藥物有效控制。然而,隨著病情進展,藥效逐漸下降,并可能誘發嚴重副作用。多巴胺細胞療法應運而生,通過向腦內移植外源性神經元,以替代喪失的vmDA神經元,成為極具前景的治療策略。該領域歷經數十年探索,從最初采用胎兒組織來源的多巴胺細胞,發展到近年利用干細胞制備的多巴胺細胞并進入臨床試驗,取得了長足進步。但與此同時,該療法也易滋生誤解。
在此背景下,2026年4月17日,國際知名期刊《帕金森病雜志》(Journal of Parkinson’s Disease)發表了一篇題為“干細胞治療與帕金森病:科學與誤解”的研究綜述[1]。
本文旨在回顧該療法的演進歷程(過去、現在與未來),在辨析常見誤解的基礎上,建立合理預期,凸顯其真正潛力,以增強學界與公眾的信心與樂觀態度,并對帕金森病多巴胺細胞療法的現狀做出批判性總結。
二、過去:胎兒組織移植——從希望到局限
2.1 早期探索與成功信號
早在20世紀80年代,科學家將大鼠胚胎腹側中腦多巴胺能(hfVM)神經元移植到帕金森病模型大鼠中,移植物存活、釋放多巴胺、改善運動障礙。隨后的人源hfVM移植在開放標簽試驗中取得了令人振奮的結果:部分患者運動評分顯著改善,甚至可停用多巴胺能藥物。
2.2 雙盲試驗的冷水
然而,20世紀90年代美國國立衛生研究院資助的兩項雙盲安慰劑對照試驗潑了冷水。療效個體差異大,且15%至56%的患者出現了移植誘發性運動障礙(GID),部分嚴重到需要深部腦刺激手術來控制。
原因何在?后來分析發現,胎兒組織中混雜了血清素能神經元,它們釋放的5-羥色胺可能是GID的元兇。此外,尸檢報告顯示,移植多年的神經元內出現了α-突觸核蛋白陽性的路易小體——帕金森病的病理可以“蔓延”到移植細胞。但需要指出,這種蔓延非常緩慢(最長存活24年的病例中,絕大多數vmDA神經元仍然健康),所以“療法必然失敗”的說法并不準確。
2.3 重新評估與患者選擇
后續研究認識到帕金森病的異質性:早期、年輕、對左旋多巴反應良好、下游神經環路完整的患者,移植效果遠優于晚期患者。這是因為他們的腦內還保留著較好的“土壤”,移植的“種子”更容易扎根整合。
但胎兒組織移植有一個根本性死結:來源不可持續。治療一個患者需要4-5個胎腦,無法標準化生產。TRANSEURO研究中,87例計劃手術因組織短缺而取消。這直接推動了干細胞衍生移植的崛起。
三、當下:干細胞移植——從分化到臨床
多能干細胞(PSC)的類型、特性與選擇困境:PSC具有無限自我更新和分化為任何細胞類型(包括腹側中腦多巴胺能神經元)兩大核心特性,主要包括胚胎干細胞(ESC)和誘導多能干細胞(iPSC)。ESC來源于囊胚期內細胞團,在部分司法管轄區存在倫理爭議;而iPSC通過強制表達多能性轉錄因子(Oct3/4, Sox2, Klf4, c-Myc)對體細胞進行重編程產生,規避了倫理問題,且可實現自體移植從而避免免疫排斥。
然而,iPSC重編程可能增加遺傳或表觀遺傳異常的風險。目前學界尚未就使用ESC還是iPSC達成共識,因此在正在進行的臨床試驗中,兩者均被用于衍生腹側中腦多巴胺能神經元。
分化方案的演進——從早期失敗到關鍵突破:早期分化嘗試通過形成表達PAX6的神經中間體(如擬胚體或共培養)產生多巴胺能神經元,但這些細胞并非特異性的腹側中腦類型,移植到6-羥基多巴胺損傷的嚙齒動物后存活率差、運動改善微弱。
關鍵突破在于發現真正的腹側中腦多巴胺能神經元起源于表達FOXA2和LMX1的神經中間體,據此開發了新方案:雙重抑制SMAD信號通路(TGF-β和BMP),同時激活SHH和經典WNT信號通路,并添加適當生長因子。由此分化的神經元在動物模型中存活率和功能顯著優于早期方案。后續研究進一步優化了生長因子的時機與濃度,并引入流式分選技術,使方案日趨成熟。
臨床轉化的安全性質疑、控制措施與初步試驗結果:上述方案已按良好生產規范(GMP)標準改進,推動了PSC衍生的vmDA祖細胞進入早期臨床試驗。然而,最大隱憂在于:即使移植極少量未分化的PSC,也可能導致畸胎瘤形成。研究表明,含有1%未分化人ESC的移植物即可在免疫缺陷小鼠中致瘤。但通過嚴格的臨床前測試與質量控制(如確保未分化細胞比例低于0.1%),可達到安全標準。目前全球至少1200名患者接受了基于PSC的細胞療法移植,迄今未見腫瘤形成報告。
2020年,首例PSC來源的vmDA祖細胞移植患者病例報告發表。該患者接受的是自體iPSC來源的vmDA祖細胞移植。盡管1?F-DOPA攝取和臨床運動評分有所改善,但最顯著的改善體現在生活質量上——患者自述生活質量顯著提高。然而,因僅治療一名患者,這些結果無法推廣,凸顯了開展涉及多名患者的早期臨床試驗的必要性。
此后,美國、中國、歐洲和亞洲各地開展了多項類似試驗(見表1),包括由英國劍橋大學與瑞典隆德大學聯合開展的STEM-PD試驗。截至撰稿時,其中三項試驗的結果已發表于同行評審期刊。



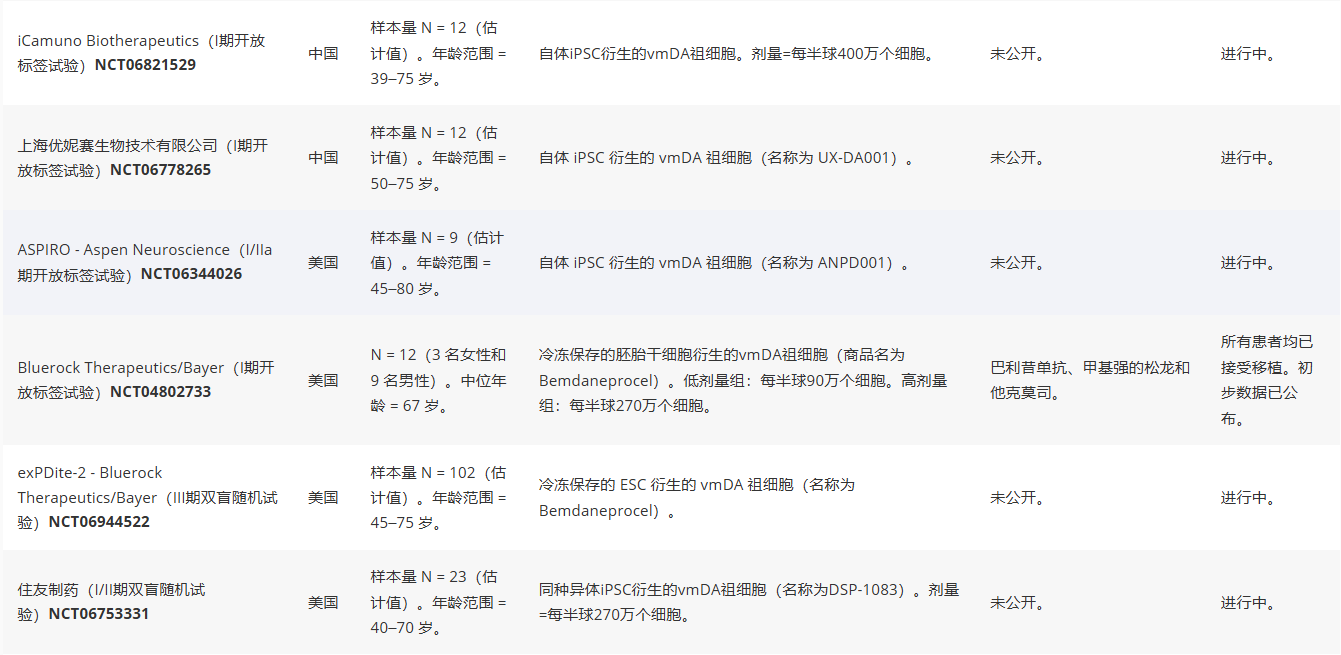
日本的一項I/II期開放標簽試驗中,患者接受了低劑量或高劑量的同種異體iPSC衍生vmDA祖細胞移植。所有患者均未觀察到異常生長、腫瘤形成或GID。后者與早期hfVM試驗中5-HT神經元污染導致GID的假設相符。然而,鑒于隨訪期相對較短,長期安全性尚不能完全排除。PET成像顯示,所有患者的1?F-DOPA攝取量均有輕微增加,高劑量組更為顯著。但高劑量組的絕對1?F-DOPA攝取值低于低劑量組,且兩組的攝取值均遠低于健康個體水平。
這表明,移植后存活并成熟為功能性多巴胺能神經元的祖細胞數量,遠未達到完全修復神經網絡所需的數量。耐人尋味的是,這與TRANSEURO試驗的結果相似——后者同樣存在個體差異,但臨床運動評分改善最大的患者,其1?F-DOPA攝取值已恢復至與健康對照組相當的水平。
為補充上述試驗,美國(Bluerock Therapeutics/Bayer)與韓國分別開展了兩項I/IIa期開放標簽試驗。患者接受了低劑量或高劑量hESC衍生的vmDA祖細胞移植。與日本試驗類似:未見異常生長、腫瘤或GID,短期安全性良好;臨床運動評分適度改善,提示潛在療效,但PET顯像中1?F-DOPA攝取量仍未恢復正常。
需要審慎指出,上述三項試驗均存在局限性:樣本量小、缺乏對照組、開放標簽設計(患者與研究者均知曉所接受的治療)。因此,其療效數據可能受到安慰劑效應和/或觀察者偏倚的影響,須謹慎解讀。盡管如此,短期安全性數據已使監管機構有信心批準更大規模的臨床試驗。
事實上,Bluerock Therapeutics/Bayer已于2025年9月啟動一項III期隨機、假手術對照、雙盲試驗。該試驗規模遠超此前的I/II期試驗,旨在更嚴格地評估hESC衍生vmDA祖細胞移植的療效,并期望在獲得積極結果后最終取得上市許可。同樣,日本試驗的更大規模后續研究也正在籌劃之中。
四、未來:攻堅克難——從存活率到非運動癥狀
盡管III期已啟動,部分學者認為為時過早——因為此前試驗中,尚無患者實現PET攝取正常化、PD藥物減量或運動評分顯著改善。因此,在開展大規模決定性試驗前,需先在小規模研究中優化以下幾個核心問題(圖1):
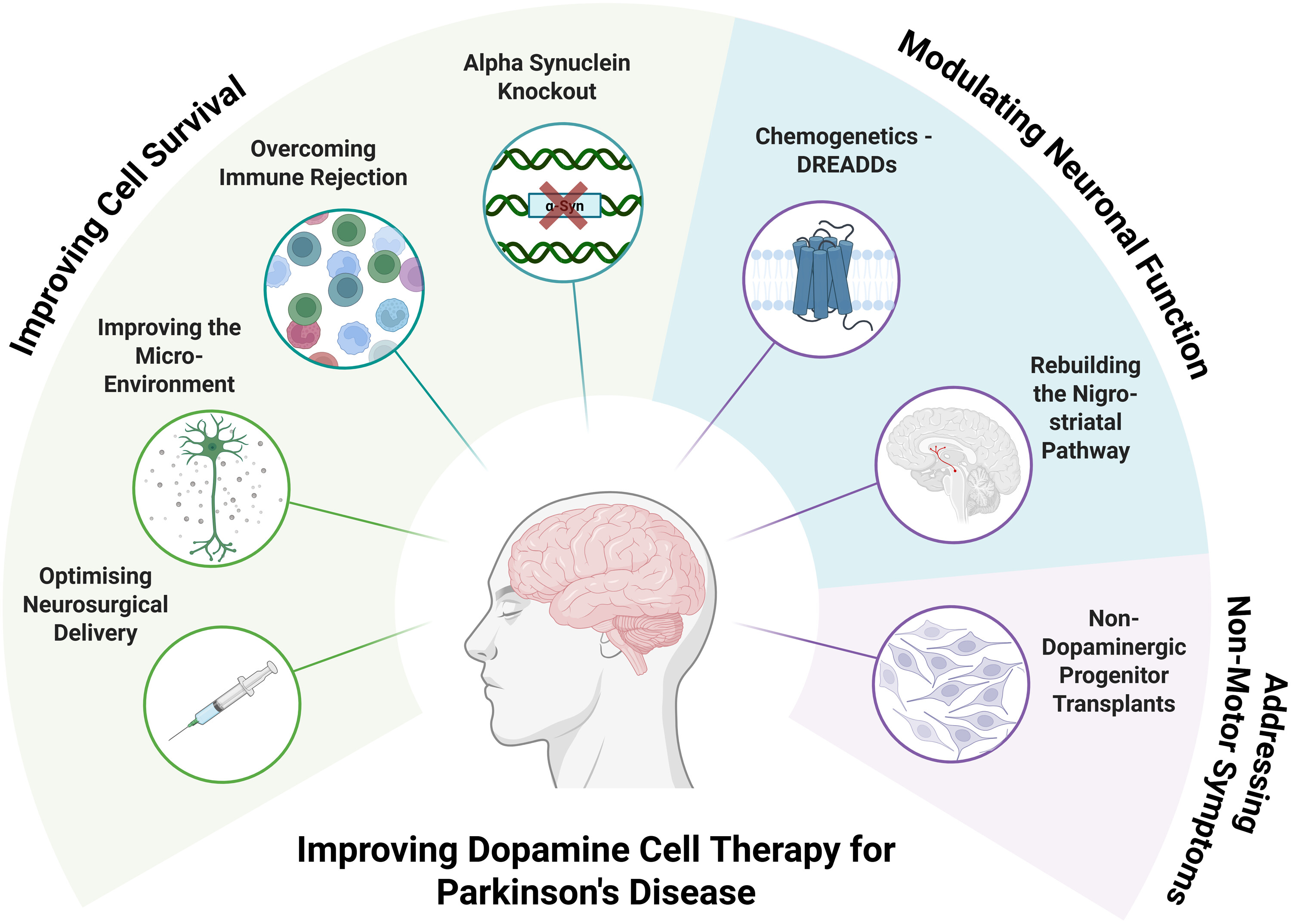
4.1 提高祖細胞存活率
目前估計移植后存活率僅約5%。增加初始劑量需要更多次腦內穿刺,每次增加約1%的血管損傷風險。亟需單次穿刺、防回流的新型注射器械。
成年大腦缺乏足夠的神經營養支持。補充GDNF可提高存活率,但會降低細胞成熟度,需要優化時機;TNF-α抑制劑阿達木單抗也被證明可改善存活。
4.2 解決免疫排斥
避免免疫抑制的三種策略:
- 自體iPSC:耗時、昂貴,無法規避散發性PD風險。
- HLA匹配庫:如英國需要約150條細胞系才能覆蓋大部分人群,成本高昂。
- 低免疫原性PSC:敲除HLA并過表達CD47。但CD47可能使惡性細胞逃避免疫監視,需引入安全開關。
4.3 調節神經元活動——化學遺傳學(DREADDs)
直接移植到紋狀體無法重建上游黑質-紋狀體環路。移植到黑質可重建,但需要長距離軸突生長(可用靶向直流電刺激引導)。
更前沿的策略是化學遺傳學:在移植細胞中導入工程化受體(如對氯氮平-N-氧化物CNO反應的Gq偶聯受體),可通過外部給藥誘導去極化、增強多巴胺釋放,改善運動功能。同時可用[11C]CNO-PET可視化表達DREADD的神經元。但基因導入存在突變風險,同樣需要安全開關。
4.4 解決非運動癥狀
當前療法僅改善部分運動癥狀,對認知缺陷、癡呆等非運動癥狀收效甚微,因為這些癥狀源于非多巴胺能神經元(如基底前腦膽堿能神經元)的退化。未來方向是聯合移植互補細胞類型——例如補充膽堿能神經元,以全面改善生活質量。
五、常見誤解與事實澄清
| 誤解 | 事實 |
|---|---|
| “胎兒移植試驗完全失敗” | 部分患者確實獲益顯著,但GID和病理蔓延問題限制了應用;且患者選擇不當是重要原因 |
| “帕金森病病理會迅速摧毀移植細胞” | 病理蔓延極其緩慢(數年至數十年),絕大多數移植細胞長期存活 |
| “干細胞移植會致癌” | 嚴格質控(未分化細胞<0.1%)下,全球1200例患者尚無腫瘤報告 |
| “移植后就能根治帕金森病” | 目前僅旨在修復運動回路、緩解癥狀,無法阻止非多巴胺能系統的退化 |
| “所有患者都適合細胞移植” | 早期、年輕、左旋多巴反應好的患者效果最佳;晚期患者受益有限 |
六、總結與展望
從胎兒組織到多能干細胞,帕金森病多巴胺細胞療法走過了數十年跌宕起伏的歷程。早期試驗的挫折促使我們更深入地理解患者選擇、細胞純度、存活率等問題;當前早期臨床試驗證實了短期安全性,但療效依然有限,PET顯示多巴胺能信號遠未恢復正常。
未來的突破依賴于多學科協作:優化細胞存活(新型器械、生長因子聯合)、解決免疫排斥(低免疫原性PSC)、重建完整環路(化學遺傳學、軸突引導)、以及聯合移植治療非運動癥狀。
III期試驗已經啟動,但在此之前,我們仍需以迭代方式開展小規模優化研究,避免重蹈“過早開展大規模試驗導致失敗”的覆轍。正如綜述作者所言:正視并克服當前方法的不足,才能防止多巴胺細胞療法再度被棄。
七、常見問題解答(FAQ)
參考資料:
[1]:Stamper A, Bulstrode H, Barker RA. Stem cell treatments and Parkinson’s disease: Science and misconceptions. Journal of Parkinson’s Disease. 2026;0(0). doi:10.1177/1877718X261434672
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信