核心速覽:間充質干細胞(MSCs)治療腦卒中等神經系統疾病,核心機制之一是促進血管新生——為缺血區建立新的血流通道。本文基于2026年《Stem Cells and Development》綜述,系統解析MSCs促血管生成的三大機制(旁分泌主導、分化輔助、細胞接觸調控),以及增強其療效的四種策略:藥物預處理(簡單短效)、基因修飾(強效高風險)、低氧/3D培養(溫和安全)、生物材料支架(解決存活難題)。臨床證據顯示,MSCs移植可改善腦卒中患者運動功能,外泌體作為無細胞療法正成為新方向。
干細胞如何促進血管新生并治療神經系統疾病?四大方法讓“血管搭橋”更高效
一、為什么MSCs能治腦中風?血管新生是關鍵
腦中風(缺血性腦卒中)后,大腦某區域的血管被堵死,下游神經元因缺血缺氧而死亡。現有的溶栓和取栓手術能開通大血管,但已經梗死的腦組織和缺血半暗帶里的瀕死神經元,需要新的微血管來提供營養、清除壞死組織。
間充質干細胞(MSCs)正好能促進血管新生——這是它治療神經系統疾病的核心機制之一,甚至比它直接變成神經元更重要。
華中科技大學同濟醫學院附屬同濟醫院神經外科團隊近期在《Stem Cells and Development》上發表了一篇綜述,系統梳理了MSCs促血管生成的機制,以及如何通過四種修飾策略讓MSCs“更強、更準、更安全”。這篇文章不僅總結了臨床證據,還指出了從“細胞療法”向“無細胞療法”過渡的趨勢[1]。
二、直接移植MSCs:臨床證據有了,但還不夠
2.1 腦卒中患者的臨床試驗
MSCs移植在腦卒中患者中已經有不少臨床試驗。
2021年,Chung團隊做了一項針對慢性重度腦卒中患者的研究。他們給患者注射了自體MSCs,3個月后整體殘疾評分(改良Rankin量表)沒有顯著改善——聽起來有點失望。但仔細分析功能細節發現,患者的腿部運動功能有明顯提升。這說明MSCs可能不是“全腦修復”,而是對特定功能區域有效。
2020年,Jaillard團隊針對亞急性腦卒中患者(發病后幾周內)做了另一項試驗。他們靜脈輸注了自體骨髓來源的MSCs,結果證實安全可行,而且患者的運動功能恢復與感覺運動神經可塑性有關。也就是說,MSCs幫助大腦重新組織了神經網絡。
2.2 直接移植的三大隱患
盡管有效,但直接往血管里打活的MSCs有三個讓人擔心的問題:
- 免疫原性:異體MSCs雖然低免疫原性,但不是零。反復輸注可能引發排斥。
- 致瘤風險:任何活細胞在體內長期存在,理論上都有變成腫瘤的可能,雖然MSCs概率極低。
- 堵塞血管:MSCs直徑約15-30微米,靜脈輸注后大部分被肺部截留,少數能到達腦部。但如果細胞團塊形成,可能堵塞梗死區已經脆弱的微血管。
這就是為什么研究者開始尋找“無細胞”的替代方案。
三、外泌體:MSCs的“無細胞使者”
3.1 外泌體是什么?
外泌體是細胞分泌的一種納米級小囊泡,直徑只有50-150納米,里面裝著蛋白質、mRNA、miRNA等生物活性分子。它們就像細胞之間的“快遞包裹”,MSCs通過外泌體把指令傳遞給其他細胞。
3.2 臨床證據:外泌體數量與療效相關
Bang等人的臨床試驗發現了一個有趣的現象:患者接受自體MSCs注射后24小時內,血液中的外泌體水平升高了大約5倍。而且,外泌體的數量與患者運動功能的改善程度獨立相關。與此同時,腦內MSCs分泌的神經營養因子水平并沒有升高。
這說明什么?MSCs的神經修復作用,很可能主要是通過外泌體介導的,而不是靠MSCs自己跑到腦子里干活。
動物實驗也證實了這一點:給缺血性腦卒中小鼠注射MSCs外泌體,這些外泌體能夠遷移到損傷腦區,顯著促進血管新生和神經發生。
3.3 外泌體的優勢
與直接移植MSCs相比,外泌體療法有幾個明顯好處:
- 無免疫排斥:外泌體沒有細胞膜表面的MHC分子,不會引起排斥。
- 無致瘤風險:不是活細胞,不會分裂增殖。
- 無栓塞風險:尺寸小,不會堵塞血管。
- 易于保存:可以凍干,不需要液氮。
所以,外泌體正在成為再生醫學領域的一個熱門方向。
四、MSCs促血管新生的三大機制
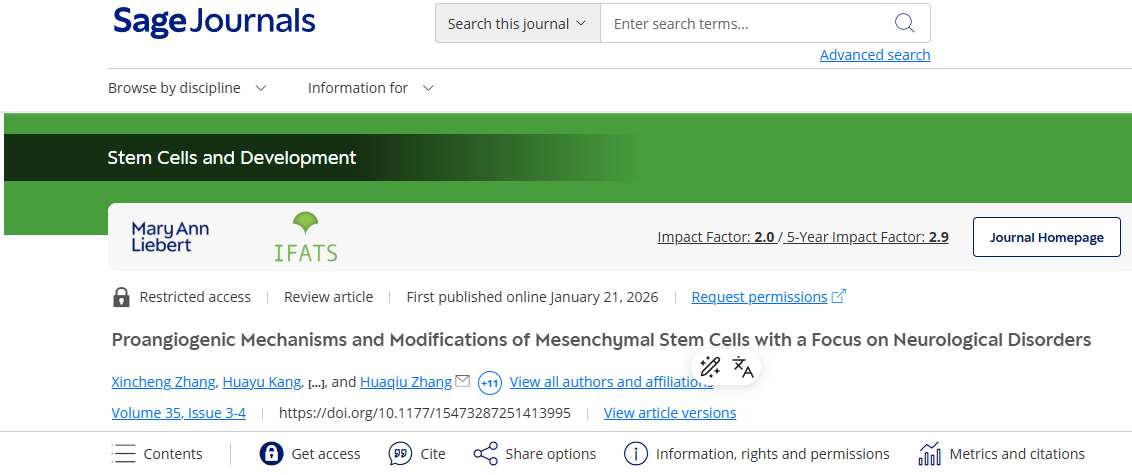
目前,MSCs主要用于治療神經系統疾病中的腦缺血性疾病(圖1)。其對急性缺血性卒中的治療機制可概括為抑制急性局部炎癥、促進長期神經功能恢復和血管重塑,其中血管重塑對患者的功能恢復至關重要。新的功能性血管結構能為梗死灶提供更多營養支持,促進局部壞死組織清除,并減輕缺血半暗帶區內神經元的缺氧狀態和代謝紊亂。
圍繞這一關鍵環節,MSCs的促血管生成機制可歸納為三個層面,其中旁分泌占據主導地位,分化與直接接觸分別作為輔助和新興補充。
3.1 第一,旁分泌作用——主導機制。
MSCs能夠分泌大量生物活性分子(包括VEGF、FGF、TGF-β等可溶性蛋白以及攜帶核酸和蛋白質的外泌體),這些旁分泌因子被釋放到局部微環境中,通過以下順序促進血管新生:首先誘導內皮細胞遷移和增殖,隨后促進管腔形成,最后募集周細胞、沉積基底膜以穩定新生血管。
實驗證據表明,僅使用MSCs的條件培養基(含旁分泌產物)即可在腦缺血模型中顯著減少梗死體積并改善神經功能,證實旁分泌效應足以產生治療效果,且無需MSCs直接存在。
3.1 第二,直接分化為內皮細胞——體外明確但體內證據不足。
在特定誘導劑(如VEGF、辛伐他汀)或機械刺激下,MSCs在體外可表達內皮細胞標志物并形成管狀結構。然而,目前缺乏MSCs在體內穩定、可控地轉分化為功能性內皮細胞的臨床證據,因此這一機制對實際血管生成的貢獻尚不明確,不是主要作用途徑。
3.2 第三,直接細胞-細胞相互作用——新發現的輔助機制。
近期3D微血管芯片模型觀察到,MSCs會選擇性地定位于血管生成芽的隆起或根部,并通過直接接觸參與毛細血管的激活與穩定。這一機制超越了傳統的旁分泌和分化范疇,提示MSCs可能通過物理接觸實時調控血管生成過程,但其在體內的普遍性和重要性仍需進一步驗證。
綜上,MSCs促血管生成并非單一路徑,而是以旁分泌為始動與主導,以分化為潛在補充(實際貢獻有限),以細胞間接觸為精細調控節點。正是旁分泌的主導地位,催生了“無細胞療法”(直接使用外泌體或條件培養基),以規避直接移植MSCs的免疫原性與致瘤風險;但無細胞療法也喪失了持續分泌和細胞接觸調控的優勢,故并非完全替代方案。
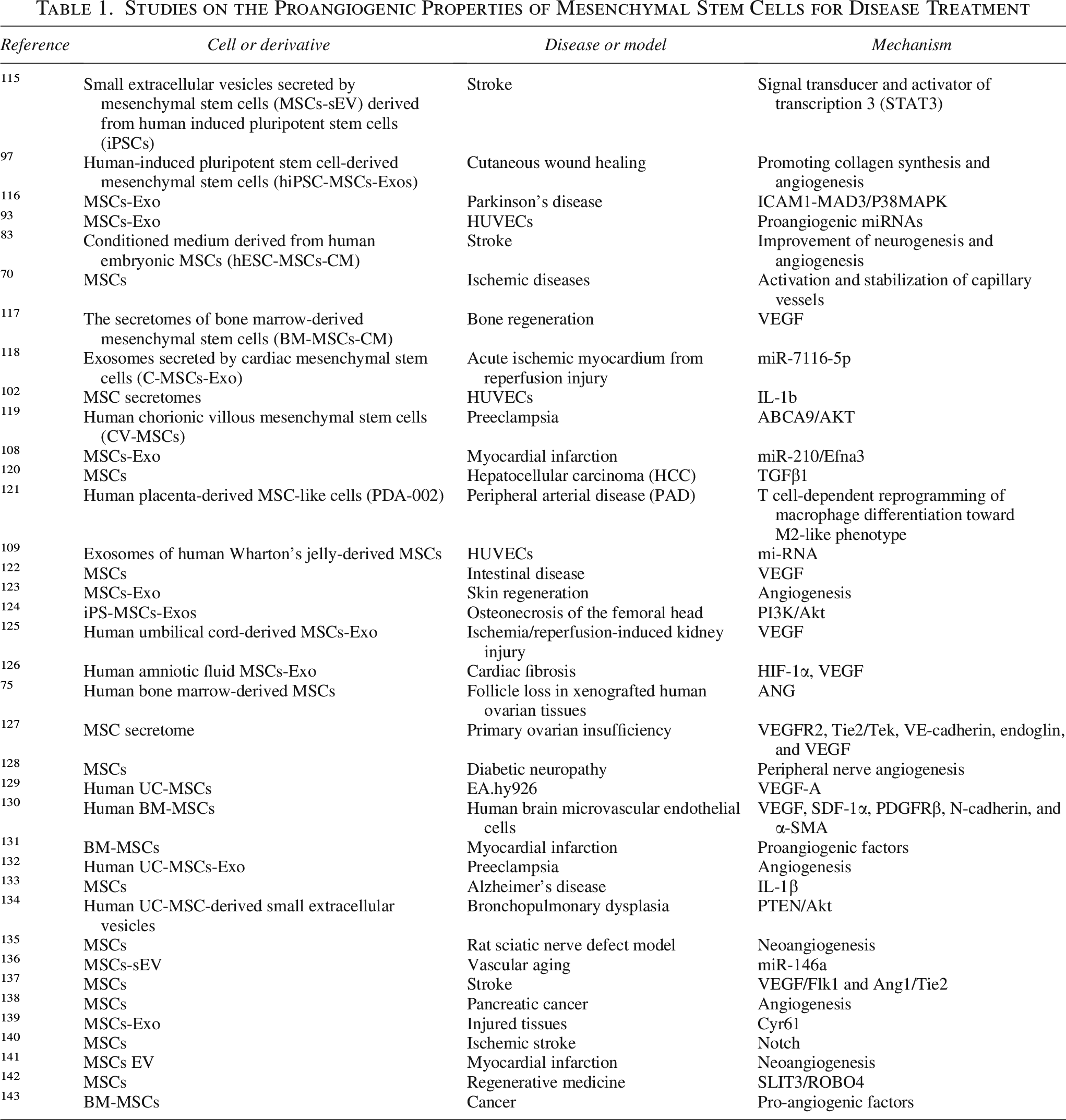
表1列出了利用MSC的促血管生成特性進行疾病治療的其他研究。
五、修飾提高間充質干細胞的療效的方法
過去20年間,MSCs已成為臨床試驗中最常用的細胞治療劑之一。ClinicalTrials.gov數據顯示,截至2025年11月28日,以“間充質干細胞”注冊的研究已達1405項。
然而,全球獲批上市的MSCs療法數量屈指可數。野生型MSCs固有的諸多缺陷,嚴重制約了其臨床應用的范圍與效果。為此,研究者正從多個維度對MSCs進行工程化改造,以提升其治療潛能。當前主流修飾策略包括藥物預處理、基因修飾、培養環境調控及聯合生物材料,各具邏輯,亦各有困境(圖2)。
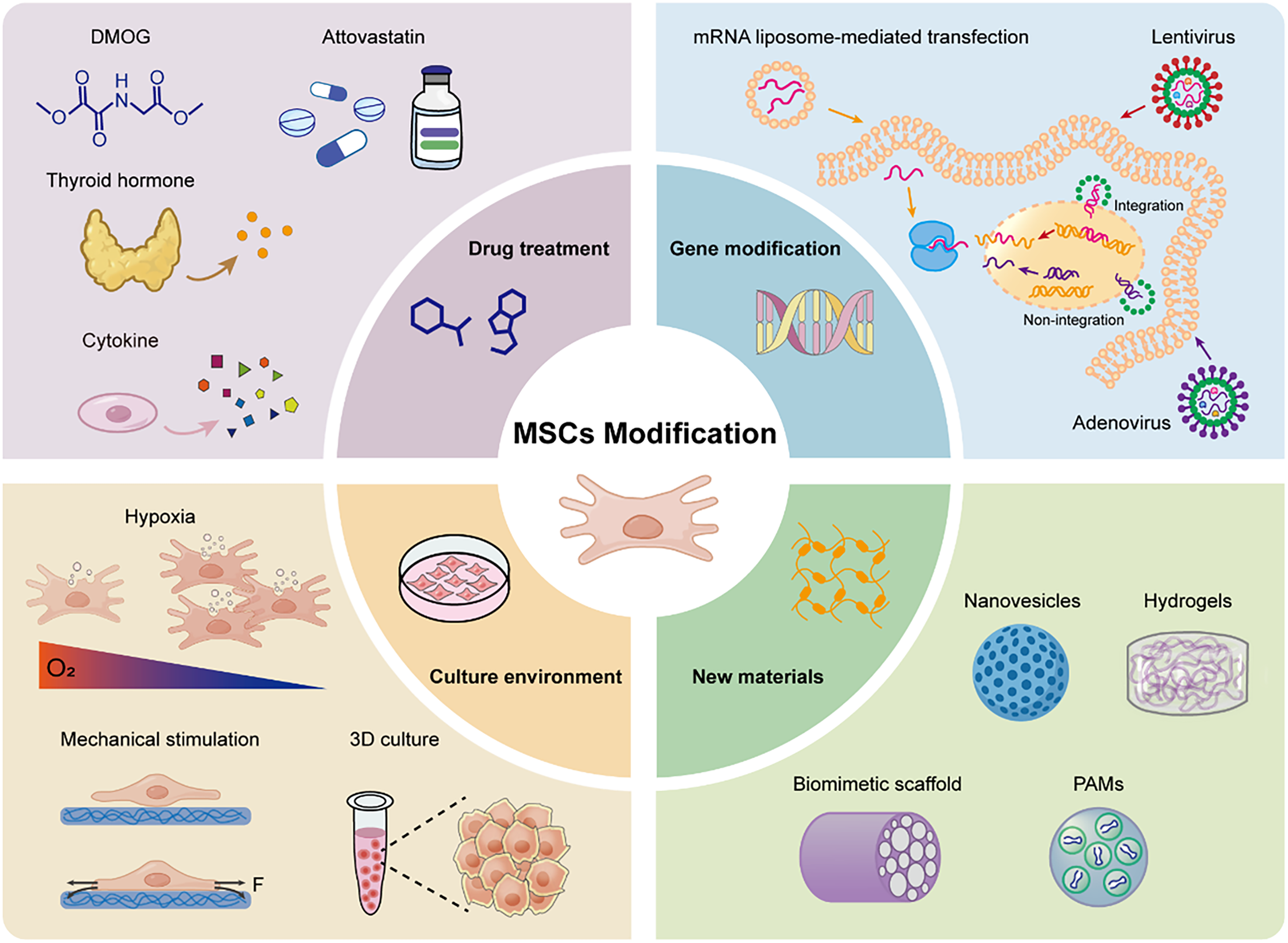
5.1、藥物預處理:短效激活,簡便易行。
間充質干細胞(MSC)對外部刺激敏感,易于接收外部信號并調節自身的生物學行為。用不同的藥物刺激MSC可以顯著改變其功能。研究發現,許多藥物可以增強MSC的血管生成功能,包括各種生長因子、細胞因子、激素和市售藥物(表2)。
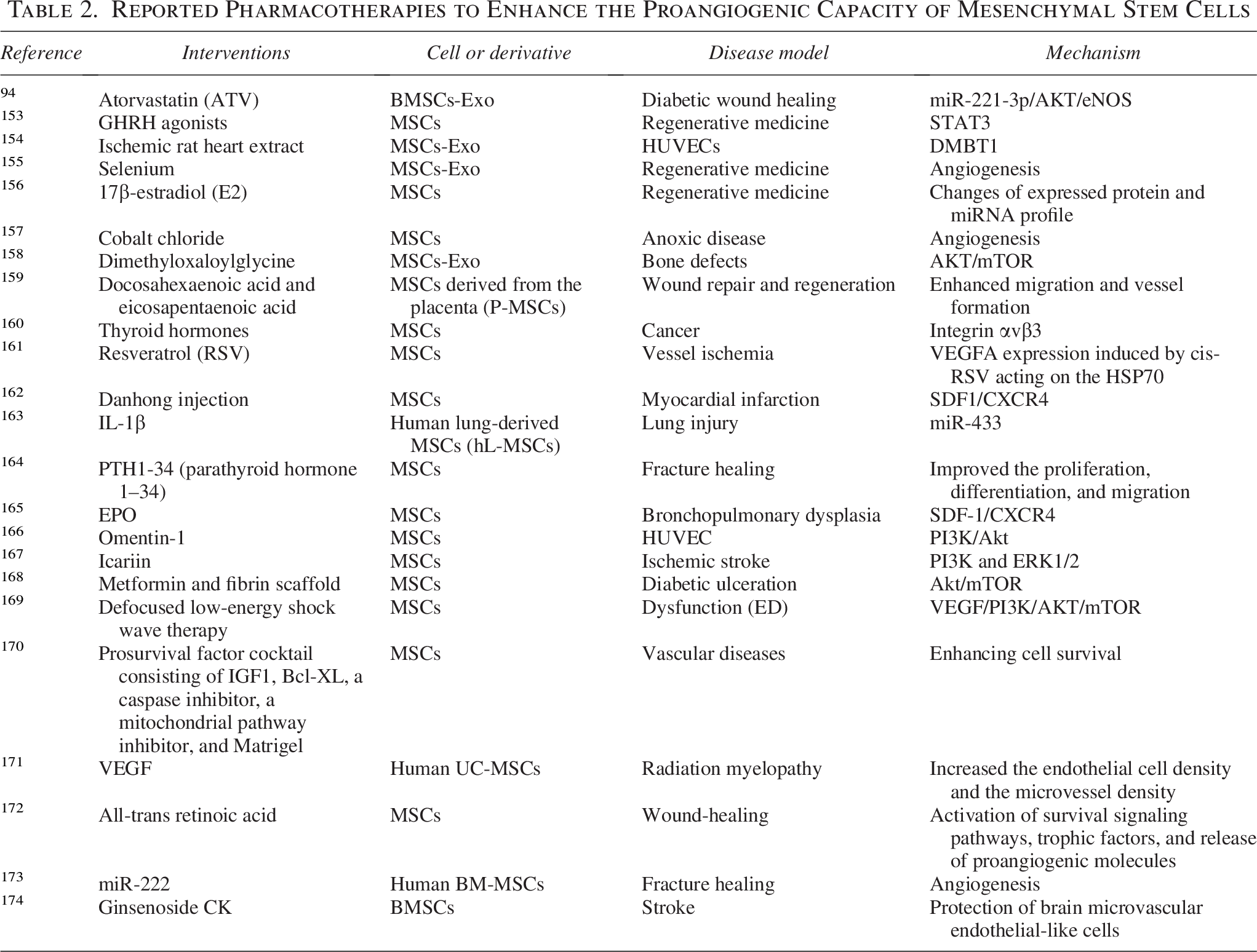
該方法最為直接——將MSCs在體外與特定藥物共孵育一段時間,實現“預激活”。例如,DMOG刺激可增強MSCs外泌體的促血管生成能力;促紅細胞生成素則通過激活SDF-1/CXCR4軸間接促進血管新生。該策略操作簡單、成本低廉,不依賴復雜基因操作設備,多數實驗室均可開展。
但其短板同樣突出:藥效短暫。藥物一旦代謝清除,細胞迅速恢復原態,移植后長期療效難以保證。本質上,這更像一劑“短效興奮劑”,而非“底層改造”。
5.2、基因修飾:底層編輯,效果最強但風險最高。
基因修飾是最常用的修飾方法,通常使用逆轉錄病毒、慢病毒或腺相關病毒對間充質干細胞(MSCs)進行基因編輯。研究者可將HIF-1α、VEGF、miR-126等功能基因整合至MSCs基因組,使其持續高表達目標蛋白。并增強其分泌治療性細胞因子、歸巢或存活的能力(表3)。
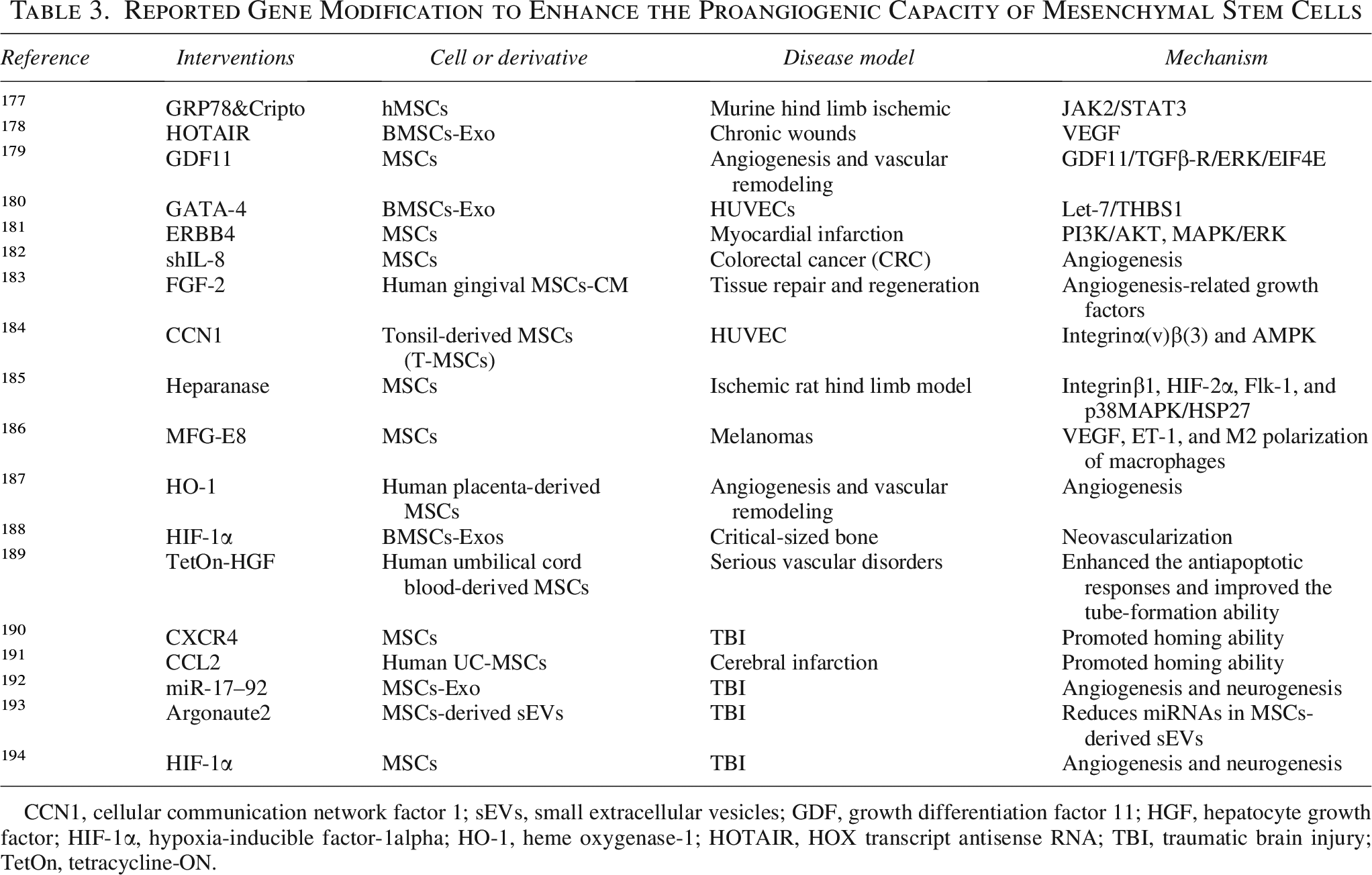
效果顯著:過表達HIF-1α的MSCs外泌體在心肌梗死模型中能顯著保護心臟功能;上調CXCR4則增強MSCs向腦損傷區域的歸巢能力。
然而,“永久性改動”伴隨隱憂——脫靶突變、插入位點不可控、潛在致瘤風險,令臨床轉化格外謹慎。一個折中策略正在興起:不再移植基因編輯后的MSCs本身,而是僅取用其分泌的外泌體,以保留增強功能的同時規避活細胞移植的安全風險。
5.3、培養環境調控:貼近生理,溫和有效。
培養環境對間充質干細胞(MSCs)的功能有顯著影響。在常規實驗室環境下,MSCs通常在21%的氧濃度下培養,但這顯然無法模擬MSCs在人體內的實際生存環境,因為MSCs在體內生存的氧濃度約為5%。因此,大量研究探討了不同培養環境對MSCs功能的影響(表4)。

將MSCs置于低氧(甚至1%氧)條件下培養,其分泌的外泌體促血管生成能力顯著提升。同樣,傳統的二維貼壁培養與體內的三維生存環境相去甚遠。采用三維培養(如球狀體或支架培養)后,MSCs分泌抗炎因子和生長因子的能力明顯增強,其外泌體促內皮細胞增殖、遷移的效果優于二維培養。
此外,循環拉伸應變、模擬腦脊液脈動等機械力干預,也被證實可上調VEGFA表達。該方法不涉及基因層面改動,相對安全,且更貼近生理狀態,在轉化研究中受到日益廣泛的關注。
5.4、聯合生物材料:解決存活與靶向難題。
MSCs移植后存活率低是長期痛點——細胞注入體內后,大部分在短期內凋亡或流失。將MSCs負載于水凝膠、藻酸鹽支架或層粘連蛋白微載體上再行移植,可顯著提高細胞的駐留與存活。更重要的是,這些材料可設計為緩釋平臺,例如預加載VEGF等信號分子,在體內形成趨化梯度,引導宿主自身修復細胞向損傷區遷移(表5)。
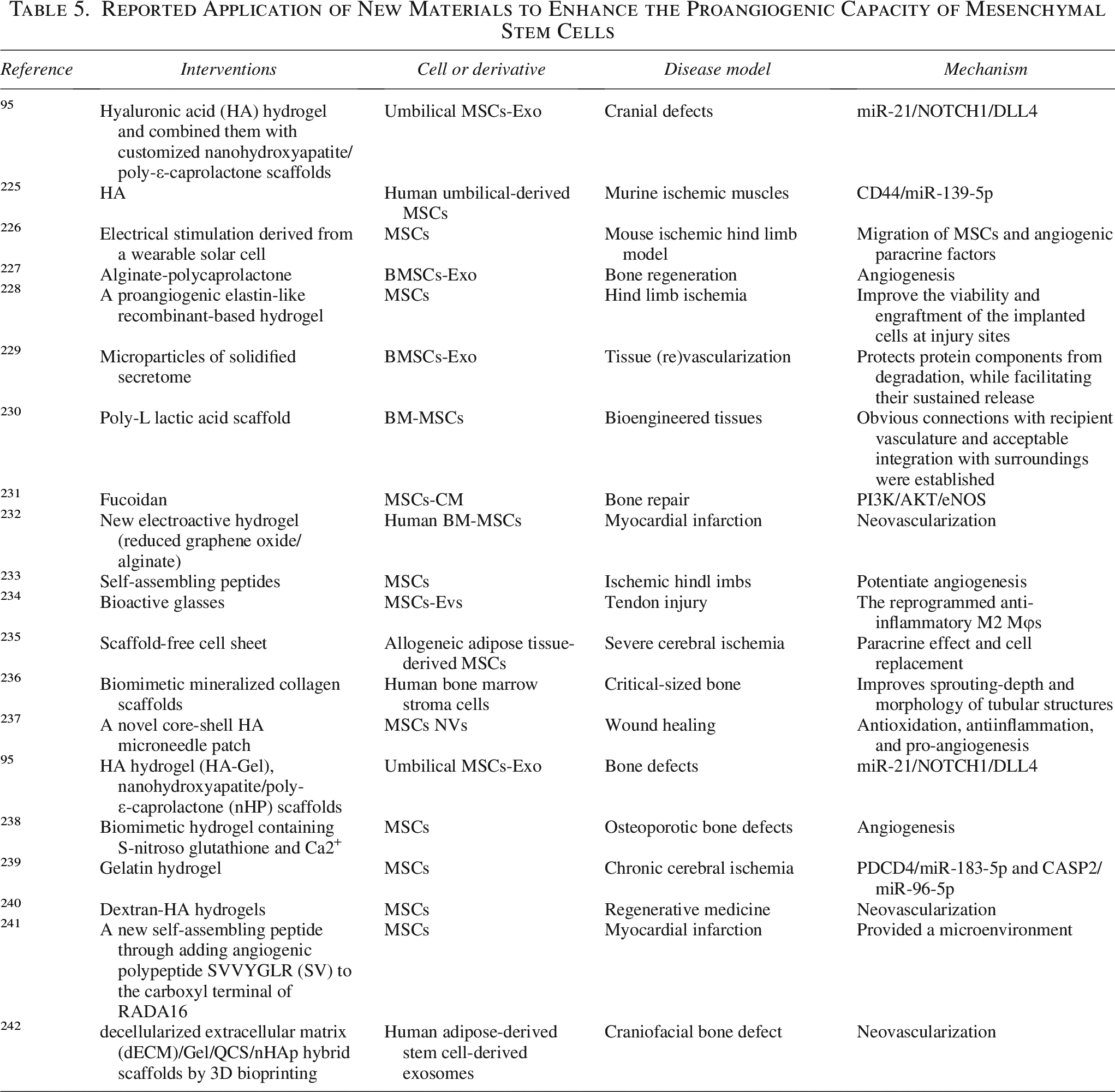
近年還涌現出更精巧的設計:給外泌體加上磁性納米顆粒,在外部磁場引導下使缺血區域的富集度提高數倍;或利用可穿戴太陽能電池產生的電刺激,引導MSCs定向遷移。這些技術的共同思路是:不再將MSCs視為孤立的“藥丸”,而是將其嵌入一個可控的遞送系統。
四大策略并非互斥。實際研究中常組合使用——例如先對MSCs進行基因修飾,再在低氧環境下培養,最后裝載于水凝膠中聯合移植。選擇何種策略或組合,取決于具體疾病模型、安全考量以及對“療效”與“可控性”的權衡。藥物預處理勝在簡單快捷,基因修飾效果最強但風險最高,環境優化溫和而有效,生物材料則聚焦于解決移植后的存活與靶向問題。尚無一種方法能兼顧所有需求——這正是該領域持續活躍的根本動力。
六、四大策略對比:怎么選?
| 策略 | 原理 | 優點 | 缺點 | 適合場景 |
|---|---|---|---|---|
| 藥物預處理 | 短時激活細胞信號 | 簡單、便宜、易操作 | 藥效短暫 | 快速增強,實驗室常用 |
| 基因修飾 | 永久性改變基因表達 | 效果最強、持久 | 脫靶、致瘤風險 | 基礎研究,外泌體來源改造 |
| 培養環境調控 | 模擬生理條件 | 安全、溫和 | 需要專門設備 | 臨床轉化潛力大 |
| 生物材料 | 提高存活和靶向 | 解決移植后流失 | 材料生物相容性需驗證 | 聯合移植,局部給藥 |
實際研究中常組合使用——比如先對MSCs進行基因修飾,再在低氧環境下培養,最后裝載于水凝膠中聯合移植。沒有一種方法能兼顧所有需求,這正是該領域持續活躍的動力。
七、總結與展望
MSCs促血管新生的核心機制是旁分泌,而不是分化成內皮細胞。它分泌的VEGF、FGF、HGF以及富含miRNA的外泌體,共同構成了促血管新生的分子網絡。
四種修飾策略——藥物預處理、基因修飾、培養環境調控、生物材料——各有優劣,殊途同歸:讓MSCs從“天生我才”走向“更強、更準、更安全”。
未來有幾個方向值得關注:
- 外泌體作為標準化產品:無細胞療法將規避活細胞的安全風險,更容易通過監管審批。
- 組合修飾:低氧培養+基因修飾+水凝膠遞送,多管齊下。
- 精準遞送:磁性導航、超聲控釋、電刺激引導,讓細胞和外泌體精準到達缺血區。
對于缺血性腦卒中等神經系統疾病,MSCs及其外泌體有望開辟一條新的“血管搭橋”之路——不是開顱搭橋,而是用細胞和納米囊泡在微觀層面重建血流通道。
八、常見問題解答(FAQ)
參考資料:
[1]:Zhang X, Kang H, Liu Y, et al. Proangiogenic Mechanisms and Modifications of Mesenchymal Stem Cells with a Focus on Neurological Disorders. Stem Cells and Development. 2026;35(3-4):47-66. doi:10.1177/15473287251413995
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信