描述:2026年《Stem Cell Reviews and Reports》綜述揭示:細胞衰老通過SASP傳播、神經(jīng)干細胞耗竭、血腦屏障破壞驅(qū)動大腦衰老。干細胞及其外泌體通過旁分泌機制恢復組織穩(wěn)態(tài),聯(lián)合衰老細胞清除劑(如D+Q)或成為抗大腦衰老的更優(yōu)方案。
修復血腦屏障、清除炎癥循環(huán):干細胞“無細胞療法”正重新定義大腦抗衰方案
2026年4月13號,知名期刊雜志《Stem Cell Reviews and Reports》“干細胞評論和報告”發(fā)表一篇“探索基于干細胞的抗衰老治療策略,以針對大腦衰老過程中的細胞衰老”的研究綜述[1]。

在這篇綜述中,我們討論了細胞衰老在神經(jīng)退行性變導致大腦衰老中的機制作用,并強調(diào)了關(guān)于干細胞及其無細胞產(chǎn)物作為潛在抗衰老治療策略的新興見解。此外,我們還強調(diào)了基于干細胞無細胞產(chǎn)物的一些治療策略,以對抗與年齡相關(guān)的大腦功能障礙。
一、什么是細胞衰老
細胞衰老是指細胞在DNA損傷、氧化應激、端粒縮短等內(nèi)在或外在應激因素作用下,永久性喪失增殖能力的一種穩(wěn)定狀態(tài)。該概念源于對衰老過程中細胞死亡率上升現(xiàn)象的觀察。
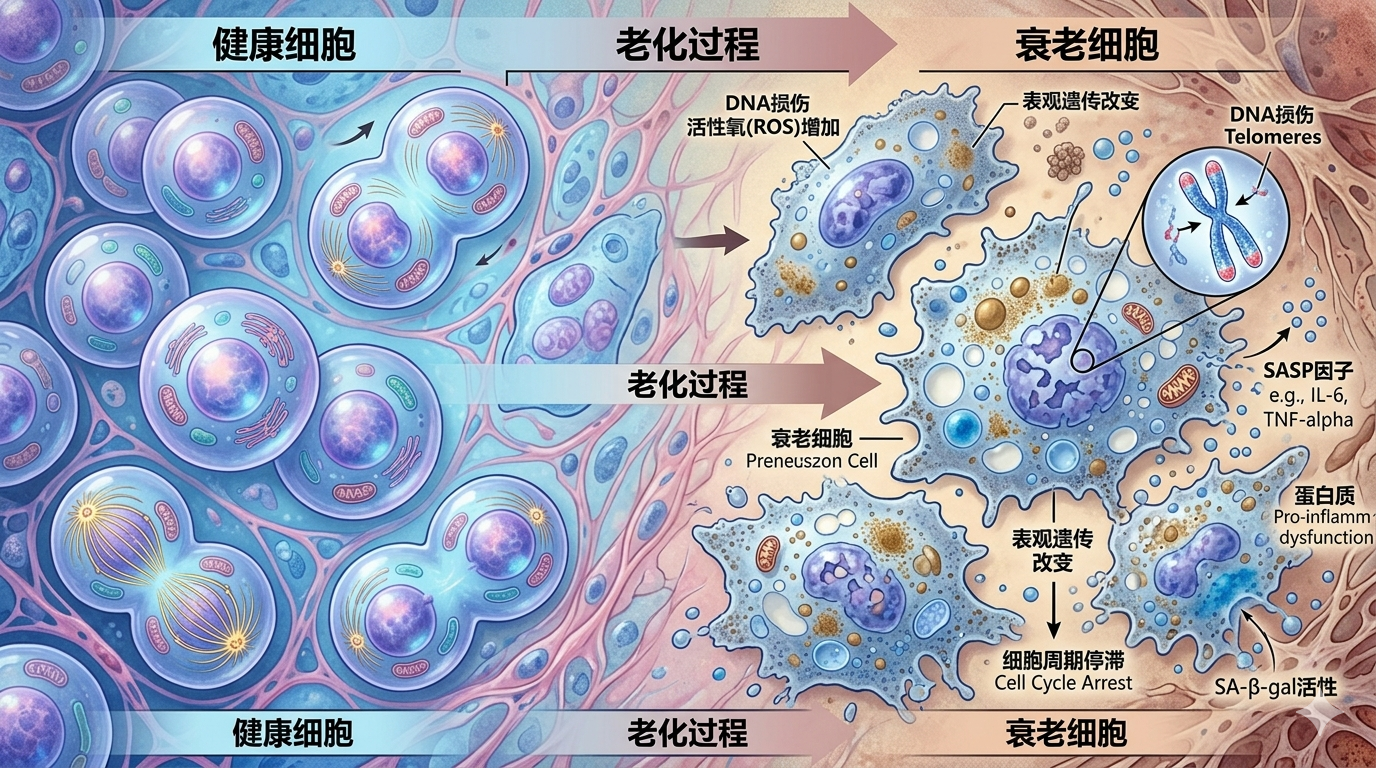
1961年,Hayflick和Moorehead通過實驗發(fā)現(xiàn)正常二倍體細胞體外分裂次數(shù)有限,即Hayflick極限,首次揭示了這一現(xiàn)象。此后,Wang進一步將細胞衰老與細胞死亡敏感性降低聯(lián)系起來。細胞衰老可響應多種信號而發(fā)生,且可獨立于端粒縮短,與生物體年齡無關(guān),因此從胚胎發(fā)生期(參與模式形成與組織發(fā)育)至成年期(協(xié)助組織修復與腫瘤抑制)均可檢測到衰老細胞,圖1總結(jié)了導致衰老的衰老細胞的各種特征。
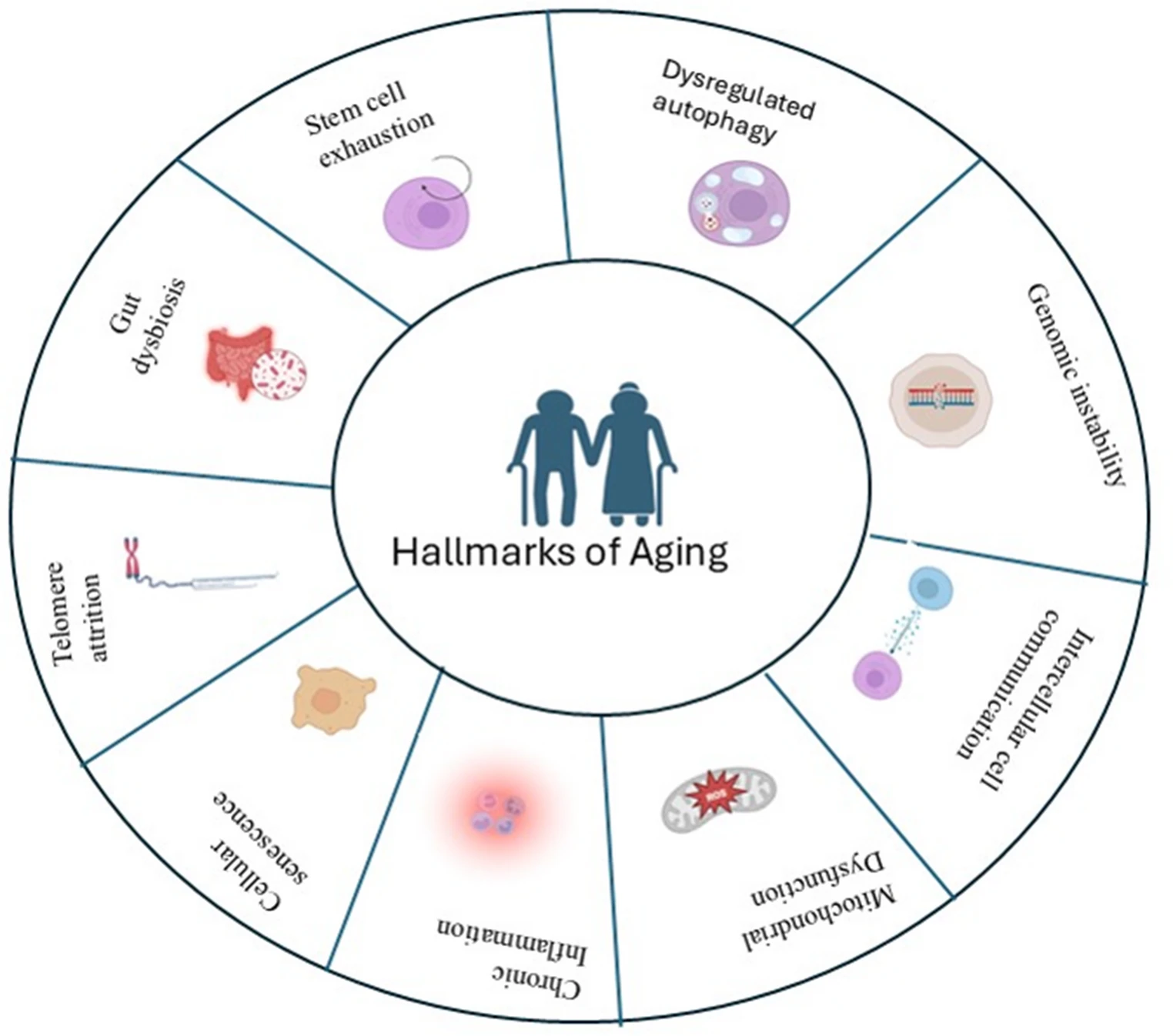
細胞衰老具有進化拮抗性多效性特征:一方面在發(fā)育、修復和抑癌中發(fā)揮有益作用;另一方面,衰老細胞會降低組織再生能力,導致機體衰老、組織退化并促進癌癥發(fā)生。
為對抗細胞衰老帶來的負面影響,已有干預措施包括選擇性清除衰老細胞的衰老細胞清除劑,以及調(diào)節(jié)衰老相關(guān)分泌表型及其下游效應的衰老細胞調(diào)節(jié)劑,從而減輕慢性炎癥并恢復組織穩(wěn)態(tài)。這些機制共同定義了細胞衰老在生物學與病理生理學中的雙重角色。
二、衰老細胞的發(fā)病機制
2.1 SASP是衰老細胞影響微環(huán)境的核心手段
衰老細胞之所以能推動發(fā)病,關(guān)鍵在于它們分泌出一整套東西,即衰老相關(guān)分泌表型(SASP)。這些物質(zhì)包括促炎細胞因子、趨化因子、基質(zhì)金屬蛋白酶和血管生成因子等。
SASP干了三件相互關(guān)聯(lián)的事:
- 第一,通過自分泌信號把自身的細胞周期阻滯穩(wěn)住,這是衰老抑制腫瘤的細胞自主機制;
- 第二,通過旁分泌信號誘導周圍的正常細胞也進入衰老狀態(tài),等于把衰老在組織里擴散開;
- 第三,把免疫細胞招過來清理衰老細胞、控制炎癥。
不過在大腦里,免疫系統(tǒng)清掉衰老的神經(jīng)母細胞反而可能損害認知功能,這說明SASP的效應因情境而異,有好有壞。正是這種旁分泌傳播能力,讓衰老從一個細胞的問題變成整個組織的問題。
2.2 神經(jīng)干細胞和膠質(zhì)細胞的衰老直接破壞神經(jīng)功能
衰老的旁分泌效應首先會波及神經(jīng)干細胞微環(huán)境。神經(jīng)祖細胞(NPC)衰老后,p16、p21、p53、γH2AX和SA-β-gal這些標志物升高,增殖標記(如Ki-67)下降,成年神經(jīng)發(fā)生逐漸減少,認知功能和組織修復能力隨之下降。
少突膠質(zhì)細胞前體細胞(OPC)衰老后分化能力受損,髓鞘合成減少,白質(zhì)退化和多發(fā)性硬化等脫髓鞘疾病更容易發(fā)生。星形膠質(zhì)細胞衰老時,GFAP和波形蛋白增加,谷氨酸清除能力下降,導致興奮性毒性;同時它們會偏向促炎的A1表型而不是保護性的A2表型,進一步推動神經(jīng)退行性變。
小膠質(zhì)細胞作為大腦的常駐免疫細胞,衰老后活性氧增多、增殖能力下降、促炎因子分泌增強,反過來激活星形膠質(zhì)細胞,形成一個自我強化的炎癥循環(huán)。膠質(zhì)細胞的衰老不僅各自為害,還相互疊加,把神經(jīng)功能的維持環(huán)境徹底帶偏。
2.3 血管衰老和血腦屏障破壞是組織惡化的結(jié)構(gòu)基礎(chǔ)
神經(jīng)功能的惡化還伴隨著血管系統(tǒng)的同步衰老。血腦屏障的完整性依賴于神經(jīng)血管單元,包括腦內(nèi)皮細胞、周細胞和星形膠質(zhì)細胞。衰老直接打擊腦內(nèi)皮細胞:緊密連接蛋白(如occludin)表達失調(diào),轉(zhuǎn)運機制改變,周細胞覆蓋減少,血管通透性增加。星形膠質(zhì)細胞的功能障礙又會加重血腦屏障的破壞(圖2)。
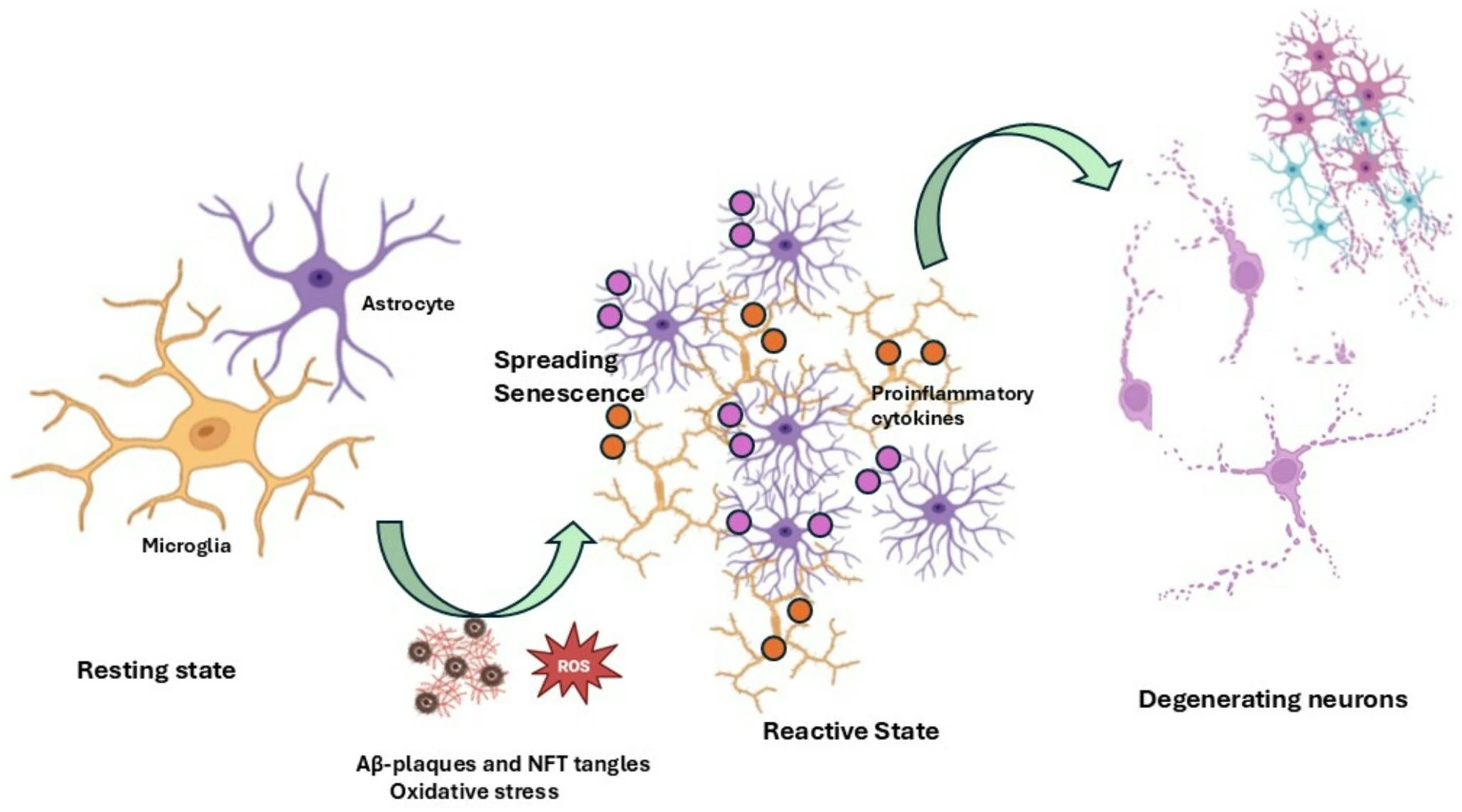
血管衰老因此成了屏障失效的關(guān)鍵推手,免疫細胞順著漏洞滲入腦組織,神經(jīng)炎癥和神經(jīng)退行性變進一步加劇。也就是說,細胞衰老不僅從功能上損害神經(jīng)和膠質(zhì)細胞,還從結(jié)構(gòu)上拆掉了血腦屏障這道防線。
2.4 炎癥衰老的正反饋和旁分泌傳播讓整個過程停不下來
以上所有機制最終匯成一個惡性循環(huán),即炎癥衰老。衰老細胞持續(xù)堆積,SASP里的IL-6、IL-1β等促炎因子把組織環(huán)境變成慢性低度炎癥。氧化應激和細胞衰老在這里互相推動:衰老產(chǎn)生活性氧,活性氧造成DNA損傷并激活NLRP3炎癥小體(小膠質(zhì)細胞是腦內(nèi)主要來源),炎癥小體再讓促炎因子成熟釋放;反過來,SASP又增強氧化應激和免疫激活,形成正反饋。
更麻煩的是,衰老還能通過旁分泌和細胞外囊泡向鄰近細胞傳播——衰老細胞的條件培養(yǎng)基就能讓受體細胞提前衰老,囊泡則遞送蛋白質(zhì)和microRNA等信號。這些機制與阿爾茨海默病等神經(jīng)退行性疾病的重疊越來越明顯,比如衰老的小膠質(zhì)細胞自噬受損,清不掉β-淀粉樣蛋白。
總之,衰老細胞通過SASP啟動、向神經(jīng)和膠質(zhì)細胞擴散、破壞血管結(jié)構(gòu)、最后依靠正反饋自維持,將大腦微環(huán)境一步步推向促炎狀態(tài),神經(jīng)元穩(wěn)態(tài)和突觸功能隨之崩潰。
這種細胞衰老、慢性神經(jīng)炎癥和旁分泌傳播之間環(huán)環(huán)相扣的機制,正好指明了治療干預的靶點。基于這些認識,抗衰老療法主要沿著三條路徑發(fā)展:直接清除衰老細胞(衰老細胞清除劑)、調(diào)控其分泌表型(衰老形態(tài)調(diào)節(jié)劑),或者通過干細胞及其產(chǎn)物恢復組織穩(wěn)態(tài)。下面就在腦衰老和神經(jīng)退行性疾病的背景下,具體討論這些策略。
三、抗大腦衰老的三大干預策略
針對上述機制,目前主要有三條路徑(圖3):
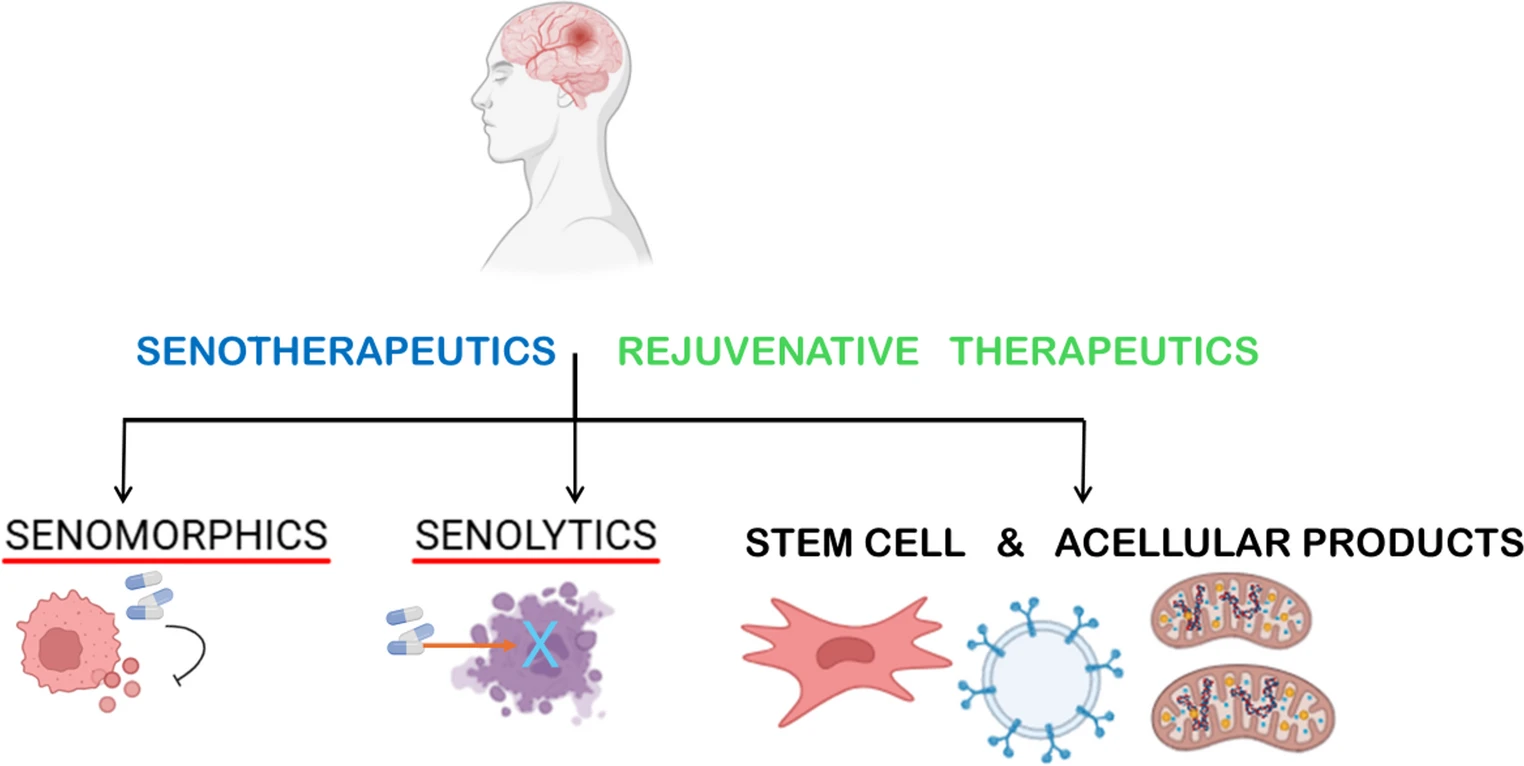
這些策略包括衰老細胞清除劑(選擇性清除衰老細胞以減輕其致病負擔)和衰老細胞形態(tài)調(diào)節(jié)劑(減少有害的衰老相關(guān)分泌表型 (SASP),但不根除衰老細胞)。至關(guān)重要的是,基于干細胞的治療被強調(diào)為一種令人振奮的新型神經(jīng)衰老治療方法。新興的基于干細胞和無細胞的再生療法通過恢復組織穩(wěn)態(tài)、減少炎癥和增強細胞修復機制,而非直接靶向衰老細胞,發(fā)揮再生和間接調(diào)節(jié)衰老的作用。與傳統(tǒng)的衰老療法相比,基于干細胞的療法可以同時針對衰老的多個方面,為與年齡相關(guān)的神經(jīng)退行性疾病提供再生和疾病改善的潛力。
3.1 衰老細胞清除劑(Senolytics):直接“掃地”
這類藥物通過抑制衰老細胞上調(diào)的抗凋亡通路,選擇性誘導它們死亡。代表藥物:D+Q(達沙替尼+槲皮素)。
在阿爾茨海默病小鼠模型中,D+Q能改善認知功能,減輕21三體綜合征相關(guān)的分子和細胞異常。非瑟酮也能進入大鼠大腦,增強海馬突觸活性來維持記憶。
這些臨床前和臨床研究給衰老細胞清除劑在神經(jīng)退行性疾病(尤其是阿爾茨海默病)里的應用提供了一些希望。表1總結(jié)了多項利用衰老細胞清除劑治療神經(jīng)退行性疾病的臨床前和臨床研究。

挑戰(zhàn):現(xiàn)有藥物對衰老細胞選擇性不夠強,可能傷及正常細胞;而且有些衰老細胞對組織修復、傷口愈合、抑制腫瘤是有益的——一刀切清除反而壞事。更合理的做法是“清除有害的,保留有用的”。
3.2 衰老形態(tài)調(diào)節(jié)劑(Senomorphics):不殺細胞,只“調(diào)音量”
衰老細胞抑制劑療法是另一種對抗細胞衰老的新型藥物療法。這類藥物能夠保護細胞免受衰老細胞釋放的SASPs的損害,且不會導致細胞死亡。衰老細胞抑制劑療法不直接殺死衰老細胞,而是通過抑制其釋放的衰老相關(guān)分泌表型(SASP)所造成的破壞性影響。根據(jù)作用模式,這類藥物分為線粒體抗氧化劑、JAK抑制劑、mTOR抑制劑、去乙酰化酶調(diào)節(jié)劑及AMPK激活劑等多個類別。
在神經(jīng)系統(tǒng)疾病方面,白藜蘆醇被證實可減少老年雌性小鼠的外周和腦部炎癥及缺血性腦損傷;富含多酚的療法則能改善老年大鼠的認知衰退和神經(jīng)功能。許多天然多酚類化合物通過減輕氧化應激、下調(diào)促炎細胞因子及活性氧積累來調(diào)節(jié)細胞衰老,展現(xiàn)出作為抗衰老治療劑的潛力。
由于該策略不引發(fā)衰老細胞裂解,僅改善其促炎分泌表型,因而在某些情境下可能比衰老細胞清除劑更為優(yōu)選。表2總結(jié)了多項利用衰老細胞類似物治療神經(jīng)退行性疾病的臨床前研究。

挑戰(zhàn):血腦屏障限制了大多數(shù)藥物進入大腦,中樞神經(jīng)系統(tǒng)生物利用度低;需要每日服用以控制緩慢積累的衰老細胞群。
3.3 干細胞及其無細胞產(chǎn)物:恢復組織穩(wěn)態(tài)
這是本綜述的重點,也是最值得展開的部分。
四、干細胞療法:從“細胞替代”到“旁分泌調(diào)控”
4.1 MSCs移植:作用機制已更新
大量研究表明,MSCs移植可促進神經(jīng)發(fā)生并恢復神經(jīng)功能,但其再生作用主要通過旁分泌因子實現(xiàn),而非直接替代死亡細胞。移植的MSCs能夠穿過血腦屏障,分泌神經(jīng)營養(yǎng)因子,遷移至損傷區(qū)域——但真正起效的是它們分泌的東西,而不是它們自己變成神經(jīng)元。
4.2 無細胞療法:外泌體(EVs)成為新寵
細胞外囊泡(包括40-159nm的外泌體)是干細胞分泌組的重要組分,在細胞間通訊中傳遞生物活性物質(zhì)(miRNA、蛋白質(zhì)、脂質(zhì))。與全細胞相比,無細胞產(chǎn)品具有更好的安全性、更易于儲存和處理,并能持續(xù)發(fā)揮生物活性。
臨床前證據(jù):
- MSCs來源的外泌體可增強海馬神經(jīng)發(fā)生
- 誘導多能干細胞(iPSC)來源的EVs能修復衰老的血腦屏障,保護老年小鼠免受缺血性中風損害
- MSCs攜帶的microRNA(如miR-17-92、miR-133b)可使衰老的神經(jīng)干細胞“恢復活力”,減少中風后認知功能下降
- 人胚胎干細胞來源的外泌體在恢復海馬功能方面具有治療潛力
4.3 已注冊的臨床試驗
綜述中列舉了多項利用干細胞及其產(chǎn)物治療年齡相關(guān)神經(jīng)退行性疾病的臨床試驗(表3,可查閱ClinicalTrials.gov,使用相應的NCT標識符)。這些試驗涵蓋了阿爾茨海默病、帕金森病、多發(fā)性硬化等適應癥,給藥途徑包括靜脈注射、鞘內(nèi)注射、鼻腔給藥等。

五、結(jié)論與展望
本綜述強調(diào)了深入理解神經(jīng)元衰老機制的重要性,這對于開發(fā)針對年齡相關(guān)神經(jīng)退行性疾病的有效抗衰老療法至關(guān)重要。干細胞具有補充神經(jīng)元群體和恢復功能網(wǎng)絡的能力,而其無細胞產(chǎn)物——如線粒體、細胞外囊泡、外泌體和分泌的營養(yǎng)因子——則提供了一種無細胞的治療途徑,從而降低了與細胞移植相關(guān)的風險。
值得特別指出的是,聯(lián)合療法,例如將衰老細胞清除劑或衰老形態(tài)調(diào)節(jié)劑與干細胞或其無細胞產(chǎn)物相結(jié)合,可能是延緩大腦衰老進程的更優(yōu)候選方案。這類聯(lián)合策略可以協(xié)同減弱神經(jīng)炎癥、增強突觸韌性、促進內(nèi)源性修復機制,從而更有效地對抗與年齡相關(guān)的認知衰退。
現(xiàn)有的證據(jù)表明,靶向細胞衰老可能為開發(fā)針對大腦衰老和年齡相關(guān)神經(jīng)退行性變的新療法提供一條充滿希望的路徑。然而,我們?nèi)孕杩朔D(zhuǎn)化醫(yī)學方面的挑戰(zhàn),包括優(yōu)化遞送方法(特別是跨越血腦屏障)、確保長期安全性以及實現(xiàn)治療方案的標準化。未來應對細胞和無細胞策略進行更深入的研究,建立分層干預方案,從而最終重新定義健康大腦衰老的治療范式。
六、常見問題解答(FAQ)
參考資料:
[1]:Sharma, P., Bhattacharyya, S. Exploring Stem Cell Based Senotherapeutic Strategies for Targeting Cellular Senescence in Brain Aging. Stem Cell Rev and Rep (2026). https://doi.org/10.1007/s12015-026-11117-5
免責說明:本文僅用于傳播科普知識,分享行業(yè)觀點,不構(gòu)成任何臨床診斷建議!杭吉干細胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請隨時聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信