炎癥性腸病 (IBD) 是一種由一系列免疫和病理生理因素引起的持續性胃腸道疾病,患者常常會遭受持續性疼痛,并面臨更高的腫瘤發展風險。在臨床中,柳氮磺吡啶是治療IBD的最常用藥物之一,但這種療法除了療效相對較差外,還可能產生一系列副作用。在某些難治性病例中,患者必須接受手術切除受累組織,這凸顯了開發更安全、更有效的替代療法的必要性。

間充質干細胞 (MSC) 近期已被證明具有強大的免疫調節活性和分化潛力,因此可能成為治療IBD的有效工具。無獨有偶,針灸作為傳統中醫瑰寶,也顯示出成為IBD有效治療選擇的潛力,在某些臨床試驗中其效果優于藥物治療。值得注意的是,針灸能夠促進內源性MSC的增殖和歸巢,使這些細胞更有效地遷移至目標病變部位并促進組織修復。
1+1>2!針灸和間充質干細胞療法相結合有望成為治療炎癥性腸病的良方!
基于這些發現,天津中醫藥大學實驗針灸科學研究中心聯合天津中醫藥大學臨床醫學系等機構人員在知名期刊《世界干細胞雜志》上發表了一篇題為“針灸和間充質干細胞療法相結合有望成為治療炎癥性腸病的良方”的綜述[1]。

該綜述系統性地闡釋了將兩種療法結合的潛在價值。首先,文章詳細剖析了IBD復雜的發病機制,這為理解MSCs的治療靶點提供了理論基礎。
間充質干細胞作為治療炎癥性腸病的前景
炎癥性腸病的發病機制:炎癥性腸病(IBD)是一種自身免疫性疾病,患者因有害免疫反應的不適當激活和相關免疫細胞浸潤而出現慢性腸道炎癥和組織損傷(圖1)。
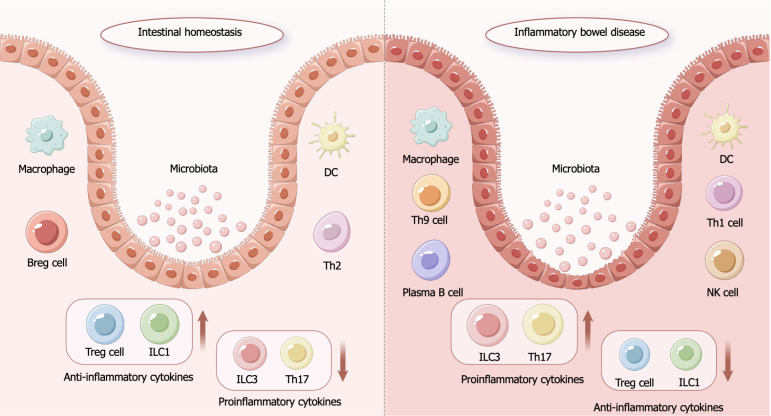
在腸道穩態下,結腸上皮結構完整,微生物被腸道屏障與腸道隔絕,機體免疫系統處于平衡狀態,腸道微環境處于穩態。在炎癥性腸病狀態下,結腸上皮結構被破壞,腸道屏障功能喪失,腸道內微生物暴露于黏膜下,促炎相關因子表達增多,從而破壞了免疫平衡和腸道微環境的穩態。
IBD的發病源于遺傳易感個體、環境因素、腸道微生物群和免疫系統之間復雜的相互作用。具有特定遺傳背景的個體,在飲食、壓力或抗生素等環境因素觸發下,其腸道屏障功能出現缺陷,導致腸道內的微生物群及其產物更容易穿透腸黏膜。這打破了腸道內固有的免疫耐受,不恰當地激活了先天性和適應性免疫系統,從而啟動了有害的免疫炎癥反應。
免疫反應的核心是多種免疫細胞的活化和細胞因子網絡的失調。特別是Th17細胞通路被證實是驅動炎癥的關鍵,與之相關的細胞因子(如IL-1β, IL-6, IL-23)大量產生,形成強烈的促炎環境。同時,多種趨化因子(如CXCL家族)濃度升高,像化學信號一樣引導中性粒細胞、巨噬細胞和淋巴細胞等免疫細胞向腸道壁浸潤和聚集,進一步放大并維持了慢性的炎癥狀態,導致組織損傷。
此外,氧化應激也是IBD發病機制中的一個關鍵環節。被激活的免疫細胞(如中性粒細胞)會產生大量的活性氧(ROS),壓倒體內的抗氧化防御系統(如超氧化物歧化酶SOD)。這種氧化與抗氧化平衡的破壞會直接損傷腸上皮細胞,破壞細胞間的緊密連接,加劇腸道屏障的滲漏,形成一個促進炎癥持續存在的惡性循環,共同導致IBD的典型病理變化。
鑒于IBD發病機制的復雜性,理想的治療策略需要同時具備免疫調節、抗氧化、抗炎和組織修復等多重功能。而間充質干細胞(MSCs)正因其具備這些全面的生物活性而成為極具前景的治療工具。
間充質干細胞的治療功能
間充質干細胞是一種分布廣泛的干細胞類型,可從脂肪組織、骨髓、子宮內膜息肉、經血甚至臍帶組織等組織中分離。除了易于獲取之外,MSCs還具有其他優勢,包括出色的自我更新能力和強大的分化潛力。MSCs能夠分化成多種細胞群,包括脂肪組織細胞和骨組織細胞。MSCs還具有強大的抗炎和免疫調節活性,能夠抑制各種炎癥疾病的癥狀,包括炎癥性腸病 (IBD) 。
MSCs的這些有益作用是通過其調節氧化應激相關信號、抑制炎癥和促進組織修復的能力來實現的,最終有助于減少疾病相關的炎癥和氧化應激。MSCs還能夠保護腸道神經系統并促進腸道屏障修復。因此,MSCs是治療包括IBD在內的炎癥性疾病的理想工具,因為它們具有多方面的治療效果。
間充質干細胞的抗氧化作用
間充質干細胞(MSCs)能夠通過調控NF-κB與Nrf2信號通路實現抗氧化,從而緩解炎癥性腸病的病理過程。一方面,NF-κB在氧化應激條件下被激活,促進炎癥因子的釋放和組織損傷,而MSCs及其外泌體可通過抑制NF-κB p65磷酸化、下調NLRP3炎癥小體的活性,從而減少炎癥反應。另一方面,MSCs可以激活Nrf2通路,促進HO-1等抗氧化因子的上調,增強機體清除自由基和維持氧化還原平衡的能力。研究還顯示,當Nrf2被敲低時,MSC外泌體的抗氧化功能顯著減弱,進一步證明了Nrf2在該機制中的關鍵作用。
在IBD的動物模型中,MSCs的抗氧化效應表現為減少氧化應激水平、保護腸道神經元并緩解因慢性炎癥導致的組織損傷。這一過程不僅體現了MSCs通過抑制炎癥因子釋放+增強抗氧化防御的雙重作用,還突出了其在維持腸道穩態、減輕組織損害方面的重要價值。因此,MSCs的抗氧化機制是其治療IBD的核心途徑之一,也是其潛在臨床應用的理論基礎。
間充質干細胞的抗炎作用
間充質干細胞(MSCs)能夠通過多層次的免疫調節機制發揮抗炎作用,從而緩解炎癥性腸病(IBD)的病理過程。
首先,MSCs可以遷移至腸道炎癥部位,直接抑制Th1和Th17等效應T細胞的活化與增殖,減少TNF-α、IFN-γ、IL-2、IL-17等促炎細胞因子的分泌;同時促進Th2細胞功能增強和IL-4的釋放,并通過分泌IL-10誘導Tregs的擴增,形成抗炎性免疫微環境。MSCs還能通過分泌PGE2抑制CD3、TNF-α、IL-2的活性,限制炎癥反應的擴大。此外,MSC分泌的IL-10、TGF-β等因子可重塑免疫應答模式,進一步推動免疫穩態的恢復。
其次,MSCs能通過與其他免疫細胞的相互作用實現間接的抗炎效應。它們可以誘導樹突狀細胞(DC)向調節性表型分化,從而減弱抗原遞呈和T細胞活化,改善實驗性結腸炎模型的病理表現。MSCs還能抑制NK細胞的增殖及TNF-α、IFN-γ的釋放,這一過程部分依賴于PGE2和IDO等可溶性因子。
與此同時,MSCs還能調節巨噬細胞表型,使促炎性的M1型向抗炎性的M2型轉變,并通過PGE2、IDO等信號通路促進Tregs增多,進一步緩解結腸炎癥。綜合來看,MSCs通過抑制促炎細胞活性、增強免疫耐受、重塑細胞間信號網絡等多重機制,實現了其在IBD治療中的顯著抗炎作用。
間充質干細胞的修復作用
間充質干細胞(MSCs)在炎癥性腸病(IBD)修復中的作用主要依賴于其歸巢能力和促進組織再生的特性。MSCs在CXCL12、CXCL4和CXCL7等趨化因子的引導下遷移至炎癥和損傷部位后,可啟動修復程序。
其一方面通過促進腸上皮細胞(IEC)的增殖并抑制凋亡,恢復腸道的結構和功能;
另一方面,MSC分泌的因子如IGF-1可激活PI3K/AKT信號通路,增強IEC的修復和再生能力,從而改善DSS或TNBS誘導的結腸炎小鼠的結腸完整性與功能。此外,MSC的條件培養基也表現出類似的促進腸道愈合作用,進一步證明了其通過旁分泌機制介導修復的潛力。
最后,也是至關重要的一點,MSCs能增強和恢復腸道屏障的完整性。它們通過來源的外泌體(如含有miR-181a)等方式,上調緊密連接關鍵蛋白(如ZO-1和Claudin-1)的表達。這些蛋白是維持腸道上皮細胞之間緊密連接的核心,它們的恢復能有效修復被破壞的腸道物理屏障,防止有害物質和微生物泄漏,從而從根本上改善IBD的病理狀態。
這些機制共同表明,MSCs通過促進上皮再生+恢復屏障穩態的雙重作用,為IBD的修復治療提供了重要支持。
針刺聯合間充質干細胞療法在IBD治療中的協同機制
針刺聯合間充質干細胞(MSC)治療炎癥性腸病(IBD)的協同作用可能涉及多層次的免疫調節和組織修復。針刺激活迷走神經-膽堿能抗炎通路,抑制脾臟和腸系膜淋巴結中促炎細胞因子(如IL-6、TNF-α)的釋放,同時增強MSC增殖。該過程進一步調節MSC分泌IL-10等抗炎介質,從而恢復腸道免疫穩態。
此外,聯合療法表現出雙重抗氧化增強作用。針刺刺激顯著降低髓過氧化物酶和丙二醛(MDA)水平,而間充質干細胞(MSC)通過抑制Nrf2/NF-κB/NLRP3信號通路來緩解氧化應激。同時,針刺激活PI3K/AKT軸,促進腸道屏障完整性的恢復。MSC歸巢至受損腸黏膜后,通過刺激腸上皮細胞(IEC)增殖啟動修復功能。
這些研究結果共同表明,針刺聯合MSC療法的多靶點修復能力可確保腸道屏障的結構重建。
針灸與間充質干細胞結合可達到更佳治療效果的機制
MSCs能夠歸巢至損傷部位是其發揮治療作用的前提,但其全身性給藥的歸巢效率較低是影響療效的關鍵挑戰。針灸則能從以下三個方面顯著提升MSCs的功能:
第一,針刺能夠通過激活SDF-1/CXCR4信號軸來誘導MSCs的歸巢。研究顯示,電針刺激可以顯著上調損傷組織和MSC表面SDF-1與CXCR4的表達,形成趨化因子梯度,從而增強MSCs的遷移能力和定向性。這種調節不僅改善了MSCs的歸巢效率,還促進其在損傷區域的富集(圖2)。
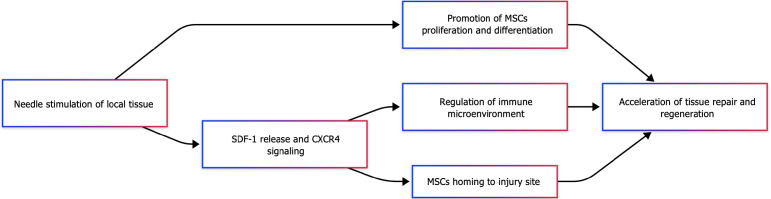
第二,針刺還可通過增強生長因子的分泌來間接促進MSCs的歸巢與存活。電針刺激能夠誘導MSCs分泌表皮生長因子等旁分泌因子,改善局部微環境,調節受損組織周圍細胞的增殖與存活,從而為MSCs的黏附和整合提供有利條件。
第三,更重要的是,針刺與MSC治療具有協同抗炎作用。電針能夠降低NF-κB的活化和下游炎癥因子(如IL-6、TNF-α)的水平,與MSC的免疫調節作用相疊加,顯著減輕炎癥反應。這種雙重作用既優化了MSCs的歸巢微環境,也使MSCs在局部能夠更好地發揮功能。
綜上所述,針刺對MSCs的促進作用體現在三個方面:
提升外源性MSCs療效:在脊髓損傷等動物模型中,電針不僅能提高移植MSCs的存活率,還能激活局部微環境,促進神經營養因子(如NT-3)的釋放,從而顯著增強MSCs向功能細胞分化的能力。
動員內源性MSCs:刺激特定穴位(如LI-11, Du-20等)可促使骨髓中的MSCs釋放到外周血液循環中,為組織修復提供了額外的細胞來源。
優化IBD治療微環境:在IBD治療中,它通過上述SDF-1/CXCR4軸提高MSCs的歸巢效率,并通過調節炎癥微環境(如增強抗炎的Treg細胞和IL-10,抑制巨噬細胞活化)來為MSCs的存活和分化創造有利條件。針刺既能直接改善腸道環境,又能增強內源性和外源性MSCs的修復功能,共同促進腸黏膜屏障的修復。
迄今為止已發表的研究已證明,針灸與間充質干細胞 (MSC) 療法相結合能夠有效治療炎癥性腸病 (IBD),針灸能夠促進MSC的增殖、分化和移植。針灸可誘導損傷部位局部釋放SDF-1并使其進入血液,從而誘導MSC表達CXCR4,從而提高其歸巢和分化能力。除了各自的益處外,MSC與針灸相結合療法還可以通過針灸刺激和動員內源性MSC和其他具有修復功能的細胞,顯著改善腸道環境(圖3)。
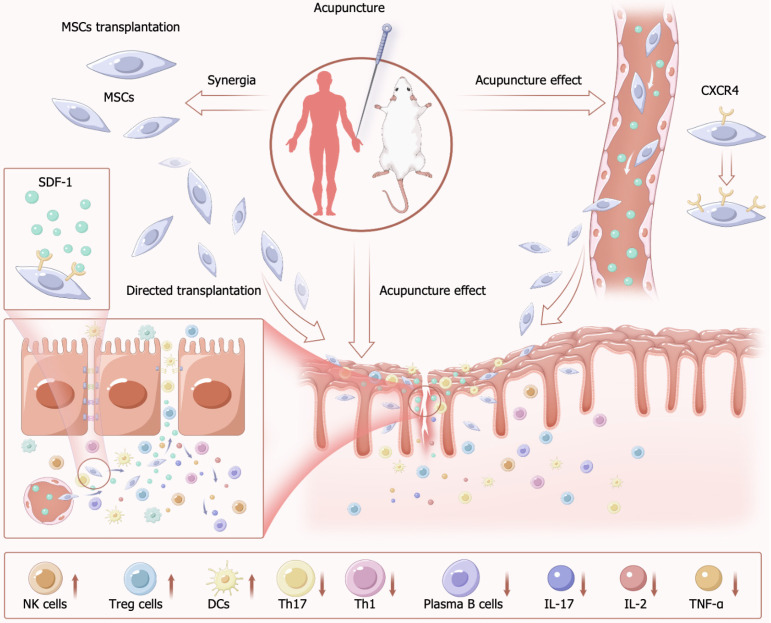
針灸能夠直接改善腸道微環境,調節炎癥活動。它還可以增強MSC反應,通過直接增強Treg和IL-10反應來抑制炎癥,同時抑制巨噬細胞的活化,從而促進腸粘膜和附近血管的修復。因此,針灸可以改善IBD癥狀,同時促進更有效的MSC移植。
總結與展望
回顧現有文獻發現,針灸作為一種擁有三千多年歷史的傳統中醫療法,在治療炎癥性腸病(IBD)方面可取得顯著療效,其鎮痛、抗炎和免疫調節機制已得到現代研究的證實。已證實 MSCs 因其抗氧化、抗炎和神經營養活性以及修復腸道屏障的能力而在治療IBD時發揮其治療益處,針灸治療IBD的能力也是如此。
因此,將MSCs與針灸相結合可提供治療IBD的協同方法,解決MSCs遷移效率低的難題,并通過多靶點、多層次的作用機制,實現1+1>2的治療效果,為未來IBD的治療提供了極具轉化潛力的新方向。
參考資料:
[1]:Ma WG, Si YX, Zhang YL, et al. Combining acupuncture and mesenchymal stem cell therapy offers promise as a treatment for inflammatory bowel disease. World Journal of Stem Cells. 2025 Jul;17(7):105371. DOI: 10.4252/wjsc.v17.i7.105371. PMID: 40740536; PMCID: PMC12305152.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信